
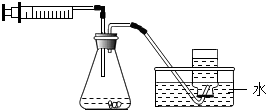
 在实验室里,利用下列物质和装置制取气体的方法正确的是( )
在实验室里,利用下列物质和装置制取气体的方法正确的是( )| A. | 二氧化锰和氯酸钾制取氧气 | B. | 大理石和稀盐酸制取二氧化碳 | ||
| C. | 大理石与稀硫酸制取二氧化碳 | D. | 锌和稀硫酸制取氢气 |
分析 此装置中的发生装置是固液常温型,反应物应为固体与液体,反应条件为常温,收集装置是排水法收集,说明该气体不易或难溶于水.
解答 解:此装置中的发生装置是固液常温型,反应物应为固体与液体,反应条件为常温,收集装置是排水法收集,说明该气体不易或难溶于水.
A、氯酸钾和二氧化锰是固体,反应条件是加热,发生装置应选用给固体加热装置,故错误;
B、大理石是固体,稀盐酸是液体,反应条件是常温,发生装置选用固液常温型装置,二氧化碳能溶于水,不能用排水法收集,故错误;
C、实验室中一般不用大理石与稀硫酸反应制取二氧化碳,以防生成的硫酸钙附着在碳酸钙的表面阻止反应的发生,故错误.
D、锌排在金属活动性顺序表中氢的前面,和稀硫酸反应生成氢气,氢气难溶于水,可以用排水法来收集,故正确.
故选D.
点评 反应物是固体与液体,反应条件是常温,可用固液常温型装置;不易或难溶于水的气体可用排水法收集.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaCl、NaNO3、KNO3、(NH4)2SO4 | B. | H2SO4、HCl、AgNO3、Na2SO4 | ||
| C. | KMnO4、CuCl2、Fe2(SO4)3、NaNO3 | D. | K2SO4、NaCl、K2CO3、NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 有机物:甲烷、乙醇、乙酸 | |
| B. | 混合物:石油、稀硫酸、冰水共存物 | |
| C. | 合成材料:合金、合成橡胶、合成纤维 | |
| D. | 复合肥料:硝酸钾、碳酸氢铵、磷酸氢二铵 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
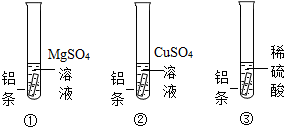
| 实验步骤 | 实验现象 | 结论 |
| 向滤出的固体中加入稀硫酸 | 固体部分溶解有红色固体剩余,产生气泡 | 固体中含有铜和铝. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com