
下列物质中,属于纯净物的是




A.茶饮料 B.蒸馏水 C.苹果醋 D.纯牛奶
B 【解析】 试题分析:蒸馏水中只含有一种物质水,是一种纯净物。故选B.科目:初中化学 来源:河北省2018学年初三毕业生升学文化课考试化学试卷 题型:单选题
如图是探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧橡皮塞,一周后观察。下列推断错误的是( )
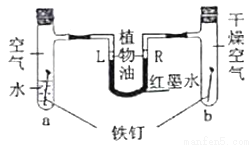
A. b管中铁钉不会锈蚀 B. 该实验说明铁锈蚀与氧气和水都有关
C. L端液面比R端高 D. 若将a管中的水改为食盐水能加快铁的锈蚀
B 【解析】A. 铁生锈是铁与氧气、水共同作用的结果,b管中铁钉不会锈蚀,正确; B. 据控制变量原则,该实验a、b中都有氧气,不能说明铁锈蚀与氧气有关,错误;C. a中铁生锈消耗氧气,使容器内气体减少,压强变小,b内不具备生锈的条件,所以气体不减少,压强不变,所以最终a中的压强比b中的小,L端液面比R端高,正确; D. 盐溶液的存在会加速锈蚀,故若将a管中的水改为食盐水能加快铁的锈蚀,正确...查看答案和解析>>
科目:初中化学 来源:江苏省江阴市华士片2018届九年级下学期期中考试化学试卷 题型:综合题
工业废料石膏(CaSO4•2H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下系列研究。
一.高纯CaO的制备
【资料一】
Ⅰ.无水硫酸铜遇水变成蓝色的硫酸铜晶体。
Ⅱ.石膏(CaSO4•2H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅲ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊,还能被高锰酸钾溶液氧化而除去。
甲同学用如下装置制备CaO并验证石膏与焦炭高温反应的其他产物。

实验过程中发现:B中无水硫酸铜变蓝,C中产生_____________现象证明有SO2生成,装置_____中无明显变化和装置F中_____________现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:___________________。
二.硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如下:

【资料二】氧化钙与焦炭在高温下反应生成碳化钙和一氧化碳。
(1)反应①的化学方程式为________________。证明固体M中不含CaCO3的方法是____________________(写出实验的方法、现象)。
(2)反应②的化学方程式为(NH4)2SO4 + 2KCl ═ K2SO4↓+ 2NH4Cl,该反应能析出K2SO4晶体的原因是_______________。
(3)假设上述流程中制得的碳化钙(化学式为CaCx)固体中只含杂质CaO,乙小组同学为测定CaCx中x的值进行如下实验。
【资料三】碳化钙在空气中灼烧生成氧化钙和二氧化碳气体。
步骤一:称取3.76g样品于下图所示石英管中(测定装置图如下,夹持及加热装置省略),反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气,测得丙溶液的质量比反应前增重了4.4g。(玻璃纤维可防止固体粉末进入导管)

步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、干燥等操作得到碳酸钙固体6克。试回答下列问题:
①装置甲的作用是_______。反应完全后继续缓缓通入空气的目的是_________。
②根据步骤一、二计算该样品中钙、碳、氧的质量比为______________,计算确定CaCx的化学式(请写出计算过程)________。
③应用:丙同学经查阅资料知道实验室常用电石(主要成分为碳化钙)与水反应制取乙炔气体(发生装置如图)。经实验发现,电石与水反应非常剧烈,为控制反应的速度以得到平稳的气流,下列改进方法可行的是______。

A.改长颈漏斗为分液漏斗或注射器 B.将电石研成粉末
C.将锥形瓶置于冰水浴中 D.用饱和食盐水代替水(电石与氯化钠不反应)
品红溶液褪色 E 澄清石灰水变浑浊 2CaSO4•2H2O + C2CaO+2SO2↑+CO2↑+4H2O CaSO4+ (NH4)2CO3==CaCO3↓+(NH4)2 SO4 取样,加入足量稀盐酸,无气泡冒出 该温度下,K2SO4的溶解度小 除去空气中的CO2气体 使残留在装置内的CO2气体被丙装置充分吸收 30∶15∶2 CaC2 ACD 【解析】一、由题意“SO2能使品红溶液褪色” ...查看答案和解析>>
科目:初中化学 来源:江苏省江阴市华士片2018届九年级下学期期中考试化学试卷 题型:单选题
能源问题、环境问题成为全国两会代表们关注的焦点之一,尤其是全国很多地区出现了严重的雾霾天气,给人们的生产、生活和健康带来了严重的影响。下列有关说法错误的是
A.计入空气污染指数的指标包括PM2.5微颗粒物
B.禁止私家车出行,改乘公交车或骑自行车等
C.减少化石燃料的使用,尽可能多地开发利用太阳能、风能、地热等
D.废旧电池不能随意丢弃,应统一回收集中处理,以减少污染,同时可以回收金属资源
C 【解析】 试题分析:A、计入空气污染指数的指标包括一氧化碳、二氧化硫、二氧化氮以及PM2.5微颗粒物,正确,B、应减少私家车出行,而不是禁止,改乘公交车或骑自行车等,错误,C、减少化石燃料的使用,尽可能多地开发利用太阳能、风能、地热等,正确,D、废旧电池中含有镉、汞、铅等有害金属,故不能随意丢弃,应统一回收集中处理,以减少污染,同时可以回收金属资源,正确,故选C查看答案和解析>>
科目:初中化学 来源:北京市门头沟区2018届九年级一模化学试卷 题型:单选题
次氯酸钠(NaClO)是消毒液的主要成分。NaClO中Cl元素的化合价为
A. ﹣2 B. ﹣1 C. ﹢1 D. ﹢2
C 【解析】根据化学式中各元素正负化合价代数和为0计算解答。 钠元素显+1价,氧元素显﹣2价,设铬氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(﹣2)=0,则x=+1价。故选C。查看答案和解析>>
科目:初中化学 来源:湖南省常德外国语学校2018届九年级下学期期中考试化学试卷 题型:科学探究题
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小滨同学设计了实验,以探究碳酸氢钠的化学性质.
【探究实验1】碳酸氢钠溶液的酸碱性
【实验方案】取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞溶液,振荡。
现象:溶液变成浅红色.由此得出结论①__________________________;
【探究实验2】能与酸反应
【实验方案】取少量该固体加入试管中,滴加稀盐酸,现象为②_____________________;
【探究实验3】碳酸氢钠的热稳定性
【实验方案】用如下所示装置进行实验

现象:充分加热后,大试管口有水珠出现,管底有白色固体残留,清石灰石变浑浊.
结论:碳酸氢钠受热能生成二氧化碳、水和一种白色固体.
验证:(1)请你帮小滨设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH(所选试剂不能用酸).步骤③______________________,现象④_________________________。
(2)写出碳酸氢钠受热分解的化学方程式⑤________________________________________
【拓展应用】试说出碳酸氢钠在日常生活中的一种用途⑥___________________________。
NaHCO3溶液显碱性 固体溶解,有大量气泡产生 取样,加水溶解滴加氯化钙(氯化钡)溶液 有白色沉淀产生 2NaHCO3 Na2CO3+CO2↑+ H2O 治疗胃酸过多(合理即可) 【解析】(1). 酚酞试液是常用的酸碱指示剂,遇碱性溶液变红,遇酸性或中性溶液不变色;向碳酸氢钠溶液中滴入几滴酚酞,试液变成红色,说明碳酸氢钠溶液呈碱性 ; (2). 碳酸氢钠也盐酸反应生成氯化钠、二氧化碳、水,...查看答案和解析>>
科目:初中化学 来源:湖南省常德外国语学校2018届九年级下学期期中考试化学试卷 题型:单选题
有四种溶液:、①、氢氧化钠溶液;②硫酸钠溶液;③稀硝酸;④氯化铁溶液,不用其他试剂就可将它们逐一鉴别出来,其正确顺序是
A. ④①③②; B. ④②①③; C. ④③②① ; D. ①③②④
A 【解析】这四种物质中,④氯化铁溶液为黄色,其它三种物质的溶液为无色,所以首先鉴别出④氯化铁溶液;将④氯化铁溶液滴加到其它三种物质中时,能得红褐色沉淀的是①氢氧化钠。由于稀硝酸呈酸性可以和碱反应,所以可以将剩余的两种溶液分别和生成的氢氧化铁反应,稀硝酸酸可使其溶解。因此鉴别出各物质的顺序是④①③②,故选D。查看答案和解析>>
科目:初中化学 来源:吉林省长春市宽城区2018届九年级第一次模拟测试化学试卷 题型:综合题
在实验室里配制溶质质量分数为10%的NaOH溶液。
方法一:计算→称量固体NaOH,量取一定量水→溶解
方法二:计算→量取一定量25%的NaOH溶液和水→混匀
(1)用方法一配置100g10%的NaOH溶液,需要NaOH固体______g;
(2)方法二中用量筒取25%的NaOH溶液时仰视读数,其它操作均正确,则所配溶液中溶质的质量分数_______(选填“大于”“小于”或“等于”)10%。
10g 大于 【解析】配制溶质质量分数为10%的NaOH溶液。(1)用方法一配置100g10%的NaOH溶液,需要NaOH固体∶100g×10%=10g;(2)方法二中用量筒取25%的NaOH溶液时仰视读数,比实际少,则所配溶液中溶质的质量分数大于10%。查看答案和解析>>
科目:初中化学 来源:安徽省长丰县2018届九年级下学期第二次教学质量检测化学试卷 题型:计算题
铁钉长期放置在潮湿的环境中会生锈(用Fe2O3表示铁锈)。取10g生锈的铁钉放入试管中,用CO还原,充分反应后,称得剩余固体质量为8.8g,请计算:
(1)生成CO2的质量为__________g;
(2)此铁钉中铁锈的质量分数为__________.
3.3g 40% 【解析】(1)设生成CO2的质量为x。 Fe2O3 + 3CO 2Fe + 3CO2 反应前后固体的差量 160 112 132 160-112 x 10g-8.8g =,解得x=3.3g (2)设铁钉中所含氧化铁的质量为y。 Fe2O3 + 3CO 2Fe + 3CO2 反应前后固体的差量 160 112 160-112 y...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com