化学实验是化学学习的重要手段.由于受到实验条件的限制,导致许多实验需要改变,或者发生异常现象.
【探究一】
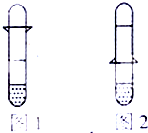
有一乡村中学由于条件所限,仅有一大一小两种试管和稀硫酸.甲(图1)、乙(图2)两学生找来铝制易拉罐皮(代替锌粒),各自设计了一种装置(如图所示),制取并收集一试管氢气.(大试管套在小试管上收集氢气)
(1)哪个学生设计的比较合理?
乙
乙
.
(2)用较合理的装置制取氢气,要使氢气充满收集氢气的试管,操作过程是
将上面的大试管慢慢地往上移
将上面的大试管慢慢地往上移
.
(3)在家里,还可以用哪些物品代替废易拉罐皮和稀硫酸完成反应?
铁钉和醋酸
铁钉和醋酸
(任写一组物质名称)
【探究二】
二氧化碳是造成地球温室效应的元凶,减少它的产生和除去它,成为每个化学工作者的重要任务.小敏、小丽、小静和我为了探究CO
2与NaOH的反应,进行了如下研究:
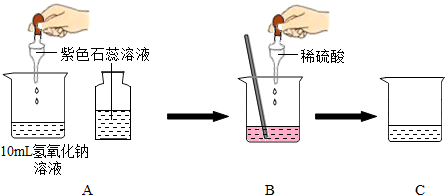
【小敏的方法】在一个充满CO
2的软塑料瓶中倒入约
体积的NaOH溶液,发现塑料瓶变瘪.小敏宣布验证了CO
2与NaOH发生了反应.
我不同意小敏的看法,理由是
二氧化碳能溶于水且能与水反应
二氧化碳能溶于水且能与水反应
;
我的做法是
设计二氧化碳分别通入氢氧化钠溶液和水的一组对比试验
设计二氧化碳分别通入氢氧化钠溶液和水的一组对比试验
.
【小丽的方法】在NaOH溶液中滴加3滴酚酞溶液,再通入CO
2,如果CO
2和NaOH溶液发生了反应,酚酞溶液应该由红色变成无色.(碳酸钠水溶液呈碱性)
我不同意小丽的看法,原因是
二者反应生成的碳酸钠显碱性,也能使酚酞试液变红
二者反应生成的碳酸钠显碱性,也能使酚酞试液变红
.
【小静的方法】将CO
2通入到NaOH溶液中一段时间,取少许反应后的液体,滴加澄清的石灰水,出现了白色浑浊.写出其中的一个化学方程式:
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
.
【我的方法】我用的物质与其他三位同学都不一样,证明反应的发生.我的实验过程如下:
实验步骤:
将CO2通入NaOH溶液一段时间,取少量反应后的液体,滴加稀盐酸
将CO2通入NaOH溶液一段时间,取少量反应后的液体,滴加稀盐酸
;
实验现象:
有气泡产生.
有气泡产生.
.
结论:CO
2与NaOH发生了反应.

 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
 化学实验是化学学习的重要手段.由于受到实验条件的限制,导致许多实验需要改变,或者发生异常现象.
化学实验是化学学习的重要手段.由于受到实验条件的限制,导致许多实验需要改变,或者发生异常现象.