
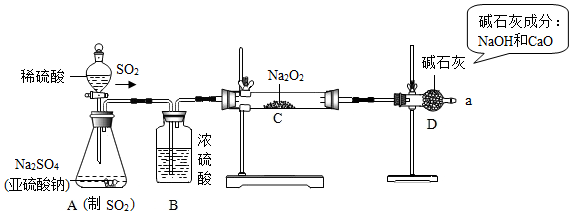
分析 【提出猜想】根据反应原理进行猜想;
【实验探究】
(1)根据反应原理写出反应的化学方程式解答;
(2)根据硫酸钠与硫酸不反应解答;
(3)根据装置A是二氧化硫的发生装置,生成的二氧化硫气体中含有水蒸气,AB间需要加一个干燥装置,避免水蒸气的存在影响探究二氧化硫和过氧化钠的反应;
(4)根据Na2O2固体的质量,利用反应的化学方程式进行解答;
【总结提升】(1)根据反应原理,利用反应的化学方程式进行有关计算;
(2)根据白色固体中含有Na2SO3,加盐酸后生成刺激性气体,利用品红褪色证明为二氧化硫解答;
解答 解:
【提出猜想】过氧化钠与二氧化硫反应的化学方程式为:2SO2+2Na2O2=2Na2SO3+O2,2Na2SO3+O2=2Na2SO4;猜想1:固体成分为Na2SO3
猜想2:固体成分为Na2SO4
猜想3:Na2SO3和Na2SO4;
【实验探究】
(1)装置图分析可知装置A中是二氧化硫气体的发生装置,反应的化学方程式为:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;
(2)打开A中分液漏斗的活塞,反应发生(产生足量的SO2)后,用带火星的木条检验从a处导出的气体,木条复燃,说明有氧气产生,而硫酸钠与硫酸不反应,故猜想2错误;
(3)水能与过氧化钠反应,则浓硫酸可干燥气体,防止水参加反应,所以B中浓硫酸作用为干燥SO2;D中可防止过量二氧化硫排放在环境中和防止空气中的二氧化碳和水蒸气进入C中;
(4)设生成Na2SO3的质量为x
2SO2+2Na2O2=2Na2SO3+O2,
156 252
78g x
$\frac{156}{78g}=\frac{252}{x}$
x=126g
Na2SO4的质量为134g-126g=8g;
【总结提升】(1)设充分反应后全部为Na2SO3+的质量为y,充分反应后全部为Na2SO4的质量为z
由2SO2+2Na2O2=2Na2SO3+O2,2Na2SO3+O2=2Na2SO4可知:
Na2O2~Na2SO3~Na2SO4
78 126 142
m1 g y z
$\frac{78}{{m}_{1}g}=\frac{126}{y}=\frac{142}{z}$
y=$\frac{21}{13}{m}_{1}$g
z=$\frac{71}{39}$m1g
则m2的取值范围是$\frac{21}{13}{m}_{1}$g<m2<$\frac{71}{39}$m1g
【总结提升】(1)
(2)白色固体中含有Na2SO3,加盐酸后生成刺激性气体,利用品红褪色证明为二氧化硫,则检验方法为将白色固体溶于水,滴加盐酸,收集气体,将气体通入品红溶液,若品红褪色,则说明含有Na2SO3,否则为硫酸钠;
故答案为:
【提出猜想】Na2SO3和Na2SO4;
【实验探究】
(1)Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;
(2)用带火星的木条检验从a处导出的气体,木条复燃;
(3)干燥SO2;防止过量二氧化硫排放在环境中和防止空气中的二氧化碳和水蒸气进入C中;
(4)126;8;
【总结提升】(1)$\frac{21}{13}{m}_{1}$g<m2<$\frac{71}{39}$m1g;
(2)将白色固体溶于水,滴加盐酸,收集气体,将气体通入品红溶液,若品红褪色,则说明含有Na2SO3;否则为硫酸钠.
点评 本题考查了物质性质的实验设计和实验验证分析判断,题目难度中等,明确二氧化硫、二氧化碳和过氧化钠性质的分析应用是解题关键,试题侧重考查学生的分析、理解能力及知识迁移能力.


科目:初中化学 来源: 题型:选择题
| A. | “超纯水”是不含任何其他物质的水 | |
| B. | “纯天然饮料”中不含任何化学物质 | |
| C. | 地球上没有水,就没有人类和所有动植物 | |
| D. | 自然界的水取之不尽,用之不竭,所以不必节约用水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 地球上的水资源是丰富的,淡水资源却很少,至约占全球水储量的5.23% | |
| B. | 空气是一种宝贵的资源,其中氮气约占空气质量的78% | |
| C. | 地壳中含量最多的金属元素是铝元素 | |
| D. | 农业和园林将喷灌改为滴灌、漫灌,可以节约用水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com