
 生活中我们经常发现存放的铁钉会生锈.
生活中我们经常发现存放的铁钉会生锈.| 实验步骤 | 实验现象 | 实验结论 | 设计实验的目的 |
| 向装有铁钉的试管中加入足量NaCl溶液,振荡 | 铁锈不溶解 | ________ | ________ |
| 实验步骤 | 实验现象 | 实验结论 |
| 向装有铁钉的试管中加入过量的铁粉 | ________ | ________ |
| 实验步骤 | 实验现象 | 实验结论 | 设计实验的目的 |
| 向装有锈铁钉的试管中加入足量的NaCl溶液,振荡 | 铁锈不溶解 | Cl-不能使铁锈溶解 | 证明Cl-(或Cl-和H2O)能不能使铁锈溶解 |
| 实验步骤 | 实验现象 | 实验结论 |
| 向取出铁钉的溶液中加入过量的铁粉 | ①无气泡出现,溶液由黄色变成浅绿色 ②有气泡出现,溶液由黄色变成浅绿色 | 溶液的组成:溶质有氯化铁(或FeCl3),溶剂是水(或H2O)或:有气泡出现,溶液由黄色变成浅绿色,或:溶液组成:溶质含有氯化氢(或HCl)和氯化铁(或FeCl3),溶剂是水(或H2O) |


科目:初中化学 来源: 题型:
 26、生活中我们经常发现存放的铁钉会生锈.
26、生活中我们经常发现存放的铁钉会生锈.

查看答案和解析>>
科目:初中化学 来源: 题型:
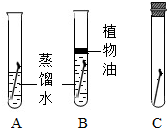
 19、生活中我们经常发现存放的铁钉会生锈.小牛和小明通过如右图所示实验对铁制品生锈的条件进行探究.通过观察和分析:得出最易生锈的是
19、生活中我们经常发现存放的铁钉会生锈.小牛和小明通过如右图所示实验对铁制品生锈的条件进行探究.通过观察和分析:得出最易生锈的是查看答案和解析>>
科目:初中化学 来源: 题型:
 21、生活中我们经常发现存放的铁钉会生锈.
21、生活中我们经常发现存放的铁钉会生锈.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
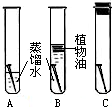 生活中我们经常发现存放的铁钉会生锈.
生活中我们经常发现存放的铁钉会生锈.查看答案和解析>>
科目:初中化学 来源:专项题 题型:实验题



查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com