
分析 (1)根据图中用到的玻璃仪器,进行分析解答.
(2)托盘天平的使用要遵循“左物右码”的原则,氢氧化钠具有腐蚀性,据此进行分析解答.
(3)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得蒸馏水的质量、体积,进而可确定所需量筒的量程.
(4)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
(5)根据称取的氢氧化钠中含有水分,实际所取的溶质的质量偏小,进行分析解答.
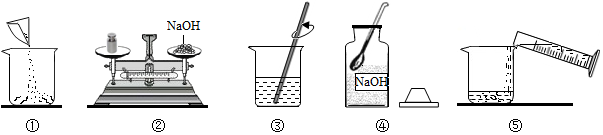
解答 解:(1)如图中的玻璃仪器分别是广口瓶、量筒、烧杯和玻璃棒.其中玻璃棒在此操作中的作用是搅拌,加快溶解速率.
(2)托盘天平的使用要遵循“左物右码”的原则,图②中氢氧化钠与砝码的位置颠倒,且没有放在烧杯中称量.
(3)溶质质量=溶液质量×溶质的质量分数,配制50g溶质质量分数为5%的NaOH溶液,需氯化钠的质量=50g×5%=2.5g;溶剂质量=溶液质量-溶质质量,则所需水的质量=50g-2.5g=47.5g(合47.5mL).选取量筒时,尽量选用能一次量取的最小规格的量筒配制时,量取47.5mL水,故应选用50mL的量筒.
(4)配制50g溶质质量分数为5%的NaOH,首先计算配制溶液所需NaOH和水的质量,再称量所需的NaOH和量取水,最后进行溶解装瓶贴签,用图示的序号表示为:④②①⑤③.
(5)若称取的氢氧化钠中含有水分,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小.
故答案为:(1)烧杯;搅拌,加快溶解速率;
(2)氢氧化钠与砝码的位置颠倒;没有放在烧杯中称量;
(3)47.5;50;
(4)④②①⑤③;
(5)偏小.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤(计算、称量、溶解)、注意事项等是正确解答本题的关键.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:初中化学 来源: 题型:选择题
| A. | 核内有22个中子 | B. | 质量为48 | C. | 核外有22个电子 | D. | 核电荷数为26 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
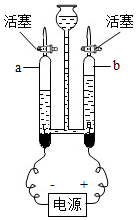 实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验.
实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
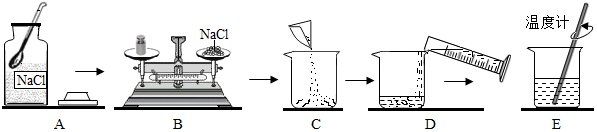
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com