
 某纯碱样品只含有氯化钠杂质.为测定碳酸钠的质量分数,称取该样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示.
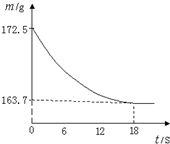
某纯碱样品只含有氯化钠杂质.为测定碳酸钠的质量分数,称取该样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示.分析 反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钠的质量和反应生成的氯化钠质量,进一步可以计算该纯碱样品中Na2CO3的质量分数和完全反应后所得氯化钠溶液的溶质质量分数.
解答 解:(1)反应生成二氧化碳的质量为:172.5g-163.7g=8.8g,
(2)设碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 117 44
x y 8.8g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{8.8g}$
x=21.2g,y=23.4g,
该纯碱样品中Na2CO3的质量分数=$\frac{21.2g}{26.5g}$×100%=80%,
(3)完全反应后所得氯化钠溶液的溶质质量分数=$\frac{23.4g+(26.5g-21.2g)}{172.5g-8.8g}$×100%=17.5%.
答案:
(1)8.8;
(2)该纯碱样品中Na2CO3的质量分数是80%;
(3)完全反应后所得氯化钠溶液的溶质质量分数为17.5%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:初中化学 来源: 题型:推断题
 A~H是初中化学常见的物质,已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,F为黑色粉末,它们的转化关系如图所示,请回答:
A~H是初中化学常见的物质,已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,F为黑色粉末,它们的转化关系如图所示,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
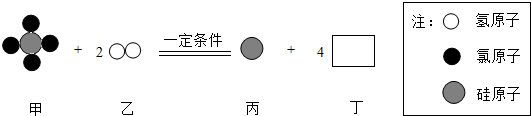
| A. | 物质丙是由原子直接构成 | B. | 甲中Si、Cl的质量比为28:142 | ||
| C. | 丁在一定条件下可转化为乙 | D. | 该反应不属于置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
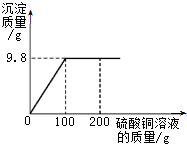 将一定质量的氢氧化钠完全溶于水形成溶液,向其中加入一定质量16%的硫酸铜溶液,测得所得沉淀与加入硫酸铜溶液质量的关系如图20所示.
将一定质量的氢氧化钠完全溶于水形成溶液,向其中加入一定质量16%的硫酸铜溶液,测得所得沉淀与加入硫酸铜溶液质量的关系如图20所示.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | MgCl2 CuSO4 KN03 NaOH | B. | H2S04 MgCl2 Fe2(SO4)3 NaNO3 | ||
| C. | Na2S04 KN03 Na2C03 NaCl | D. | NH4Cl NaCl Na2S04 NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度 | 溶解度 |
| 20℃ | 34g |
| 30℃ | 37g |
| A. | 20℃时,100g饱和KCl溶液中含有34g溶质 | |
| B. | 20℃、30℃的KCl溶液的溶质质量分数可能相同 | |
| C. | 将30℃的饱和KCl溶液降温至20℃,有3gKCl晶体析出 | |
| D. | 向相同质量的水中加入不同质量的KCl,所得溶液的浓度一定不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com