
【题目】根据下列装置图回答问题:
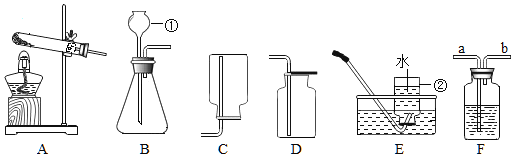
(1)写出图中标号仪器的名称①______。
(2)实验室制取并收集二氧化碳,应选用的装置组合为_________(填字母),若用F装置干燥二氧化碳气体,F中应加入的试剂是________,进气管为__________(写导管字母标号)。
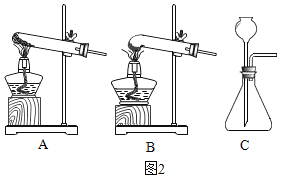
(3)加热草酸锌晶体可以制备ZnO(ZnC2O42H2O![]() ZnO+CO↑+CO2↑+2H2O),草酸锌晶体熔点为100℃,比较草酸锌晶体的熔点和分解温度,发生装置应选择图2中的装置_____(填对应装置的字母)。
ZnO+CO↑+CO2↑+2H2O),草酸锌晶体熔点为100℃,比较草酸锌晶体的熔点和分解温度,发生装置应选择图2中的装置_____(填对应装置的字母)。
【答案】长颈漏斗 BD 浓硫酸 a B
【解析】
(1)仪器①是长颈漏斗。
(2)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,同时生成氯化钙、水,属于固液常温型,所以应该选择B装置来制取二氧化碳气体;二氧化碳密度比空气大,能溶于水,应用向上排空气法收集,所以应该选择D装置来收集二氧化碳。浓硫酸具有吸水性,且不与二氧化碳反应,若用F装置干燥二氧化碳气体,F中应加入的试剂是浓硫酸;图中装置起洗气功能时进气管与出气管的方向是“长进短出”,进气管为a。
(3)加热草酸锌晶体可以制备ZnO(ZnC2O42H2O![]() ZnO+CO↑+CO2↑+2H2O),草酸锌晶体的熔点为100℃比分解温度300℃低,即还没分解就已经转化为液体,为防止液体流淌下来而不能加热,所以发生装置应选择图2中的装置 B。
ZnO+CO↑+CO2↑+2H2O),草酸锌晶体的熔点为100℃比分解温度300℃低,即还没分解就已经转化为液体,为防止液体流淌下来而不能加热,所以发生装置应选择图2中的装置 B。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:
【题目】请结合下图所示实验装置回答有关问题:

(1)写出图中标有a的仪器名称:_____。
(2)实验室用高锰酸钾制氧气的化学反应方程式为_____,为了完成该实验,还需将所选装置做出的改动是_____。
(3)实验室制取二氧化碳要求做到随时能控制反应的速率,你选择的发生装置和收集装置是_____(填序号),检验该气体所涉及的化学反应方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙的溶解度(见下表)及溶解度曲线(如下图)。下列说法不正确的是
温度/°C | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | 甲 | 26.3 | 28.2 | 31.4 | 31.4 | 30.0 | 28.2 |
乙 | 30.6 | 28.2 | 26.8 | 31.4 | 37.5 | 42.0 | |
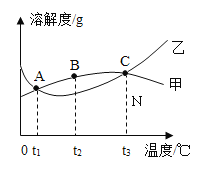
A.甲、乙为易溶物质
B.t2应介于20°C ~ 40°C
C.甲、乙饱和溶液从t3降温到t2,溶质的质量分数都变小
D.等质量的甲、乙饱和溶液从t1升温到t3,为使其溶液恰好饱和,继续添加的甲、乙固体质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年,是元素周期表问世150周年。如图中的①是钾元素在元素周期表中的相关信息。A、B、C、D、E是五种粒子的结构示意图。请根据图回答下列问题:

(1)图A中x=__。
(2)图A、B、C、D、E五种粒子共表示__种元素。
(3)C粒子的化学性质与A、B、D、E中哪一种粒子的化学性质相似?__(填选项字母)
(4)钾元素与图D所表示的元素组成的物质的化学式是__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硒元素是动物必需营养元素和对植物有益的营养元素。硒在元素周期表中的信息及原子结构示意图如图所示。下列关于硒元素的说法正确的()
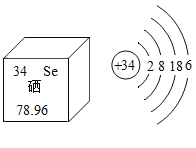
A.硒化氢的化学式是H2Se
B.硒的相对原子质量是78. 96g
C.硒在化学反应中容易失去电子
D.硒的中子数为34
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钼是稀有矿产资源,主要用于航天合金材料制作。在元素周期表中钼元素的某些信息如图所示,下列有关钼的说法正确的是
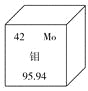
A. 原子核内质子数为42
B. 相对原子质量为95.94g
C. 属于非金属元素
D. 元素符号为MO
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】制取合金常用的方法是将两种或多种金属(或非金属)加热到某一定温度,使其全部熔化,再冷却成为合金.根据下表中的数据判断(其他条件均满足),下列合金不宜采用上述方法制取的是( )
金属 |
|
|
|
|
|
熔点 |
|
|
|
|
|
沸点 |
|
|
|
|
|
A.![]() 合金B.
合金B.![]() 合金C.
合金C.![]() 合金D.
合金D.![]() 合金
合金
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列除杂所选用试制与操作方法均正确的是
选项 | 物质 | 除杂试剂及操作 |
A |
| 加水溶解、过滤、蒸发结晶 |
B |
| 加入过量稀盐酸,蒸发结晶 |
C |
| 加入过量 |
D |
| 通入灼热的CuO |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验课上,老师知道某兴趣小组进行粗盐提纯的实验,邀请你帮助他们完成下面的实验报告。
(实验名称)粗盐的提纯
(查阅资料)
(1)粗盐中含有泥沙及少量可溶性MgCl2、CaCl2、Na2SO4等杂质。
(2)Ba(OH)2是一种易溶于水的强碱。
(主要玻璃仪器)量筒、烧杯、漏斗、玻璃棒、胶头滴管、酒精灯
(主要试剂)粗盐样品、稀盐酸、BaCl2溶液,NaOH溶液,Na2CO3溶液,蒸馏水
(实验过程)
步骤及目的 | 过程及说明 |
一、去除粗盐中的泥沙 | 1.称取粗盐样品10.0g,用蒸馏水充分溶解 2.过滤去除泥沙的溶液I 以上两步操作中均需要使用到玻璃棒,玻璃棒的作用分别是:溶解时:_______;过滤时:_______。 |
二、去除可溶 性杂质 | 将溶液I按如图流程图进行处理: 1. 加入“过量NaOH溶液时”,发生反应的化学方程式是_________。 2. 加入“过量碳酸钠溶液”发生反应的方程式是________。 3. 过滤后,所得的滤渣成分有_______种。 4. 判断“稀盐酸适量”的方法是_______________。
|
三、获得产品 | 将溶液Ⅱ注入_______(填仪器名称)中,蒸发结晶,观察到_______,停止加热,利用余热蒸干。装置完全冷却后,获得干燥的产品9.4g。 |
四、数据处理 | 该粗盐样品中氯化钠的质量分数是94% |
(结果与反思)
(1)实验操作、试剂和装置均不存在问题,老师却指出该样品中氯化钠的质量分数不是94%,原因是________________。
(2)小明提出,如果步骤二中只调换“过量的NaOH溶液”与“过量的BaCl2溶液”的加入顺序,对除杂结果也不会产生影响,你_______(填“同意”或“不同意”)小明的观点。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com