
Ϊ�ⶨʯ��ʯ��Ʒ��̼��Ƶ�����������ijѧϰС�����������ʵ��̽����ȡ10gʯ��ʯ��Ʒ�����ձ��У�����ϡ���������ٲ�������Ϊֹ��ʯ��ʯ�е����ʲ�����ˮ��Ҳ����Ӧ�����������˼���ϡ�����������ų���������������ͼ����ͼ����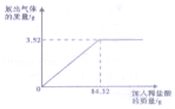
��1��̼�����ȫ��Ӧ��ȥϡ���������Ϊ�� ��g��
��2����ʯ��ʯ��Ʒ��̼��Ƶ���������Ϊ�� ����
��3���������ʯ��ʯǡ����ȫ��Ӧ��������Һ���������������Ƕ��٣����淶д��������̣�
��1��84.32��
��2��80%��
��3��������Һ�����ʵ���������Ϊ10%��
���������������1��ͼ���ת�۵��Ƕ���ǡ�÷�Ӧ�ĵ㣬�۲�ͼ���֪��ʱ��ȥϡ���������Ϊ84.32g��
��2����ͼ���֪������Ʒ��������ᷴӦ���ɶ�����̼3.52g��
��̼��Ƶ�����Ϊx�����ɵ��Ȼ�������Ϊy
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 111 44
x y 3.52g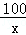 =
=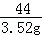 x=8g
x=8g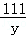 =
=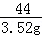 y=8.88g
y=8.88g
��ʯ��ʯ��Ʒ��̼��Ƶ���������=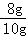 ��100%=80%
��100%=80%
��3����Ӧ���Ȼ�����Һ������Ϊ��84.32g+10g��3.52g����10g��8g��=88.8g
������Һ���������������ǣ�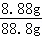 ��100%=10%
��100%=10%
���㣺���ݻ�ѧ��Ӧ����ʽ�ļ��㣻�й��������������ļ��㣮
������������һ������ͼ�����Ŀ�����ʱע�����ͼ�����㡢ת�۵���յ㼰�仯���ƣ�������ת�۵�ͨ���ǻ�ѧ��Ӧǡ����ɵĵ㣻��Ӧ��������Һ�����������������dz��л�ѧ�����һ���ص���ѵ㣬���㷴Ӧ����Һ�������ķ���һ���ǣ���Ӧ����Һ������=��Ӧǰ����ݵ�����֮�ͩ�����������������������ʣ���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��Na2CO3��NaCl��������22.3g�����ձ��У�����182.1gϡ����ǡ����ȫ��Ӧ����û��������������ձ���ʣ������������Ϊ200g������㣺
��1�����ɶ�����̼��������_________ ��
��2����������Һ�����ʵ����������Ƕ��٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
ʵ��������һ��������������ͭ��ͭ�ۣ�ͬѧ�����ⶨ���ͭ���е���ͭ�������������ֳ�ȡ20g��Ʒ�����ձ��У���ε�����������Ϊ10%��ϡ���������岻�ټ��٣�����ϡ����49g���Լ��㣺���������������ͭ��ͭ���е���ͭ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�ڹ�ҵ��ȡ����Ĺ����У��з������·�Ӧ��4FeS2+11O2 2Fe2O3+8SO2�����к�FeS260%�Ļ�����100t���������ʲ��μӷ�Ӧ������������SO2���ٶ֣�����Է���������FeS2��120 SO2��64��
2Fe2O3+8SO2�����к�FeS260%�Ļ�����100t���������ʲ��μӷ�Ӧ������������SO2���ٶ֣�����Է���������FeS2��120 SO2��64��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
ij������������15%������������Һϴ��һ����ʯ�Ͳ�Ʒ�еIJ������ᣬ����������������Һ40g��ϴ�Ӻ����Һ�����ԡ���һ����ʯ�Ͳ�Ʒ�к�H2SO4�������Ƕ��٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
ʵ�������ⶨһƿ��ǩ�����ϡH2SO4������������������ȡ10gϡ������Ʒ����5%��NaOH��Һ��μ��뵽��Ʒ�У��ӱ߽��裬����NaOH�ܶμ��룬��ҺҺ��pH�ı仯��ͼ��ʾ���Իش�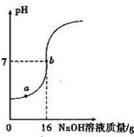
��1��a����Һ�к��е�������____________________________��
��2����pH=7ʱ������NaOH��Һ��NaOH������Ϊ____________��
��3������ϡH2SO4����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��50g 98%��Ũ��������450gˮ�У�������Һ�����ʵ���������Ϊ
| A��9.8% | B��10.2% | C��10.8% | D��19.6% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
Ϊ�ⶨʯ��ʯ��̼��ƵĴ��ȣ�ȡһ��������ʯ��ʯ���������ʲ�����ˮ�������ᷴӦ������Ҳ���ֽ⣩�� ��������һ��ʱ���õ� 78g ���壬 �ù����� 400g ���ʵ���������Ϊ 14��6%��ϡ����ǡ����ȫ��Ӧ���˵õ�20g��������ʯ��ʯ��̼��Ƶ���������Ϊ
| A��74��4% | B��80% | C�� 83��8% | D��92��6% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��202 g����ͭ��Һ�м���һ��������ǡ����ȫ��Ӧ�������ˡ���ɣ��õ�����Ĺ�������16 g������ԭ��������������Ƕ��٣����õ���Һ���������������Ƕ��٣�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com