

���� ��1�����ݳ������������Ʒ�����������˫��ˮ��ȡ�����Ļ�ѧ��Ӧ����������ʵ��ʱ��ע��������������ݹ�Һ����ķ���������
��2�������ռ�����ķ���������
��3�����ݰ��������ʼ��ռ�����������
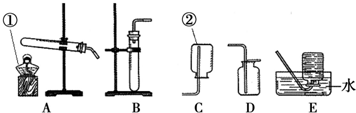
��� �⣺��1��ͼ������a�������Ǽ���ƿ���������ռ����壻����װ��B��ȡ����ʱ��������˫��ˮ�ڶ������̵Ĵ��������ڳ��������¾��ֽܷ���ȡ��������Ӧ�Ļ�ѧ����ʽ��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����ʵ��ʱ����ƿ�ڳ���©��Ҫ����Һ�����£���ԭ���Dz����ò����������ܵ���ʵ����������ù��˵ķ����������ƿ�еĹ������ʣ��������ƿ��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2������ֹ�����������ܵ������ˣ�
��2������ˮ���ռ�����ʱ����ȷ˳���ǣ�������ƿע��ˮ���ò����Ǹ���ƿ�ڣ�������ʢˮ��ˮ���У��ȵ����������Ҿ���ʱ���ٽ����ܿ����뼯��ƿ��������ƿ�ڳ���������ϲ���Ƭ���Ƴ�ˮ�ۣ��ʴ�Ϊ���ۢڢ٣�
��3������������ˮ�����Բ�������ˮ���ռ��������������ռ������ڰ������ܶȱȿ���С������Ҫ�������ſ������ռ�������Ҫ��D���ü����Ȼ�狀���ʯ�����ֹ���Ļ�������Ʊ�����������Ҫѡ��A���ʴ�Ϊ��AD��
���� ��ѧ����ʵ��Ϊ������ѧ�ƣ����Ҫѧ�����ʵ�顢����ʵ�顢����ʵ�飬Ϊѧ�û�ѧ֪ʶ�춨������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ͣ�pH=5�� | B�� | ����������pH=1�� | C�� | ���ʣ�pH=3�� | D�� | ���ӣ�pH=4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ľ�����Ա���ǿ��������Ʒ������Ʒ��������ʴ | |
| B�� | ˮ������������Ԫ����ͬ�������ߵĻ�ѧ������ͬ | |
| C�� | ���������ɲ�ͬ��Ԫ����ɵĴ������ֻ����һ��Ԫ�ص�����һ�����ǻ����� | |
| D�� | ̼������������������������ᷴӦ���������һ����̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ժ���Ʒ�����ࡢ���ࡢ���ࡢС��ʳ��Բ�����������п����Ԫ�� | |
| B�� | ���úͿ���̫���ܡ����ܡ����ܵ�����Դ���Խ�Լ��ʯȼ�ϣ���Ч����̼�ŷ� | |
| C�� | ѧ����ʳ�ö����Դ����д���������һ������Ʒ���ٽ��������Խ�Լ��Դ���������� | |
| D�� | Ϊʹֲ��ľ�Ҷ����ïʢ�������ʳ����������ʹ������[CO��NH2��3]�Ȼ�ѧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

| ���ܵ�ԭ�� | ʵ�鲽�� | ʵ������ | ʵ����� |
| ԭ��һ�� | ����Ľ�����ȷ | ||
| ԭ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
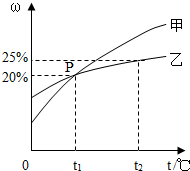 �������ֹ�̬���ʵı�����Һ�����������������أ����¶ȣ�T���Ĺ�ϵ��ͼ��ʾ��
�������ֹ�̬���ʵı�����Һ�����������������أ����¶ȣ�T���Ĺ�ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com