
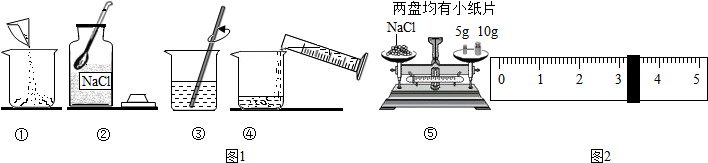
分析 (1)图①操作为把称取的氯化钠倒入烧杯,图②的操作为用药匙取氯化钠,图③操作为用玻璃棒搅拌溶解氯化钠,图④操作为把量取的水倒入盛有氯化钠的烧杯中,图⑤操作为称取氯化钠;根据利用固体溶质氯化钠配制溶液的步骤,对操作进行排序;
(2)溶解时玻璃棒的作用是加速固体溶解;
(3)砝码与游码的质量和为所称氯化钠的质量,游码读数时应以游码左侧数值为准;利用所称取溶质氯化钠的质量和所要配制溶液的溶质质质量分数,根据溶质质量分数计算公式,求出所要配制溶液的质量,溶液质量与溶质质量差即为溶剂水的质量,进而确定水的体积.
解答 解:(1)根据用固体溶质氯化钠配制溶液的步骤:计算-称量-溶解,先取氯化钠进行称取,倒入烧杯;然后量取水,倒入盛氯化钠的烧杯中;最后进行溶解;
故答案为:②⑤①④③;
(2)溶解时玻璃棒的作用是加速固体溶解;
故答案为:加速氯化钠溶解;
(3)砝码的质量为10g+5g=15g,游码的质量为3.2g,所称取氯化钠的质量=15g+3.2g=18.2g;
所配制溶液的质量=18.2g/10%=182g,则需要水的质量=182g-18.2g=163.8g,由于水的密度是1g/mL,故需要水的体积为:163.8mL;
故答案为:163.8
点评 本题对使用氯化钠配制溶液实验进行了考查,其中涉及溶液配制的步骤、溶液组成的计算、天平的使用,难度不大


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 时间/h | 2 | 4 | 6 | 8 | 10 | 12 | 24 |
| 实验1 | 不褪色 | 不褪色 | 不褪色 | 由稍褪色到褪色且速度逐渐加快 | |||
| 实验2 | 不褪色 | 不褪色 | 不褪色 | 不褪色 | 不褪色 | 褪色且速度加快 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 都需要加热 | B. | 都需要催化剂 | ||
| C. | 都有元素化合价的升降 | D. | 都有氧化物生成 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸中一定含氧元素 | B. | 含氧的化合物一定是氧化物 | ||
| C. | 盐中一定含金属元素 | D. | 碱中一定含氢元素和氧元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com