

分析 (1)根据物质的状态的变化和能量之间的关系分析回答;二氧化碳能与水化合生成碳酸,碳酸显酸性;根据气体的溶解度与压强、温度的关系分析回答.
(2)①根据碳酸氢钾的化学性质回答;②根据信息“在合成塔中,若气体X是H2,反应生成甲醇(CH3OH)和水”书写.
解答 解:(1)二氧化碳气体转变为液体时将会释放能量;二氧化碳能与水化合生成碳酸,碳酸显酸性,所以,二氧化碳使海水酸度增加,反应的方程式是:CO2+H2O═H2CO3;二氧化碳在深海中的溶解度比在通常状况下的水中的溶解度大,原因是:深海压强大、温度低,气体的溶解能力随之增强.
(2)①碳酸氢钾不稳定,受热易分解成碳酸钾、水、二氧化碳,方程式为2KHCO3$\frac{\underline{\;高压\;}}{\;}$K2CO3+H2O+CO2↑;
②根据信息“在合成塔中,若气体X是H2,反应生成甲醇(CH3OH)和水”可知,反应物是氢气,另外还有分解池产生的二氧化碳,条件是一定压强、一定温度、催化剂,产物是甲醇和水,方程式为:3H2+CO2$\frac{\underline{\;\;\;\;\;\;\;\;\;\;\;\;\;催化剂\;\;\;\;\;\;\;\;\;\;\;\;\;}}{一定压强、一定温度}$CH3OH+H2O.
故答案为:(1)释放;CO2+H2O═H2CO3;大;液体压强随着深度的增加而增加;(2)①2KHCO3$\frac{\underline{\;高压\;}}{\;}$K2CO3+H2O+CO2↑;②3H2+CO2$\frac{\underline{\;\;\;\;\;\;\;\;\;\;\;\;\;催化剂\;\;\;\;\;\;\;\;\;\;\;\;\;}}{一定压强、一定温度}$CH3OH+H2O.
点评 了解温室效应造成的后果,知道防止温室效应要从两个方面考虑:①减少二氧化碳气体的排放,②吸收二氧化碳:植树造林.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
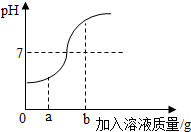 (1)该反应的化学方程式为:H2SO4+2NaOH=Na2SO4+2H2O.
(1)该反应的化学方程式为:H2SO4+2NaOH=Na2SO4+2H2O.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO2分子有碳元素和氧元素构成 | |
| B. | 干冰和二氧化碳气体都是由相同分子构成的 | |
| C. | 分子在0℃停止无规则运动 | |
| D. | 显微镜下可以看到化学变化时分子没有重新组合 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
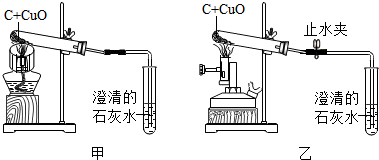
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
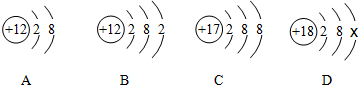
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | -2 | B. | +2 | C. | -4 | D. | +4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com