ij��ѧ��ȤС������ʦָ���£������ˡ�H
2O
2����O
2�Ŀ�����ʲô�����йء���ʵ�飮��������ش��������⣮��ʵ�����20�������½��У�
��1�����ù�������Ͷ����������������ķ�Ӧ����ʽΪ��
���ò��������к���������˳���ǣ�����װ�õ������ԡ���ˮ���д��ռ������С�Թ�ע��ˮ��
��
��
��
��
��
��
��
��
��ѡ����ţ����ٴ��������ȶ���������ˮ���� ���������е��ܵĵ�����
������Թ��ڵ����������������ټ�������MnO
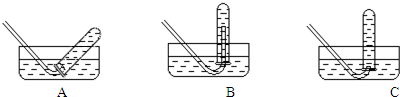
2��ĩ���Թܽ�����ˮ������ʱ��������ͼ��ʾ��3�ֲ��������к�������
C
C
��
��Ҫ֤��MnO
2�Ǹ÷�Ӧ�Ĵ���������Ҫ����ʵ������֤MnO
2�ڷ�Ӧǰ��Ļ�ѧ���ʺ�
����
����
�Ƿ�ı䣮
��2������H
2O
2����O
2�Ŀ�������������йأ�����ƿ�����6%��H
2O
2��Һ�зֱ������ͬ����MnO
2�ͺ�ש�ۣ�����������һƿ����ͬ�����O
2����Ҫ��ʱ�䣮��¼�������£�
| ʵ���� |
1 |
2 |
| ��Ӧ�� |
6% H2O2 |
6% H2O2 |
| ���� |
1g��ש�� |
1g MnO2 |
| ʱ�䣨s�� |
152 |
35 |
�ɴ˵ó��Ľ�����
����ͬ�����£�H2O2����O2�Ŀ�������������й�
����ͬ�����£�H2O2����O2�Ŀ�������������й�
��
��3������H
2O
2����O
2�Ŀ����벻ͬ����������H
2O
2��Һ�йأ�
�ڲ�ͬ����������H
2O
2��Һ����ʵ�飮��¼�������£�
| ʵ���� |
1 |
2 |
3 |
| H2O2��Һ�������������� |
5% |
10% |
20% |
| MnO2��ĩ������g�� |
0.2 |
| �ռ���500mL����ʱ����ʱ�䣨s�� |
205 |
80 |
9 |
| ��Ӧ����Һ���¶ȣ��棩 |
39 |
56 |
67 |
��ʵ���е�֪�÷�Ӧ�Ǹ�
����
����
��Ӧ������ȡ������ȡ�������Ӧ��H
2O
2��Һ���������������ӷ�Ӧ��Һ���¶���
����
����
������ߡ����͡�����H
2O
2��Һ����������������Ӱ�췴Ӧ������
����ͬ�����£�����������Һ�����ʵ���������Խ��Ӧ����Խ��
����ͬ�����£�����������Һ�����ʵ���������Խ��Ӧ����Խ��
��
��4��������Щ���ؿ���Ӱ��÷�Ӧ������
��˵�����һ�����룺
������������ʱ���ı�˷�Ӧ���¶ȣ���Ӱ��˷�Ӧ������
������������ʱ���ı�˷�Ӧ���¶ȣ���Ӱ��˷�Ӧ������
��

 =80g��������������Ϊ100g-80g=20g���������Ͷ��������������Ϊ��20g��80g=1��4����������ж����������������Ϊ��
=80g��������������Ϊ100g-80g=20g���������Ͷ��������������Ϊ��20g��80g=1��4����������ж����������������Ϊ�� =80%�����1��4��80%��
=80%�����1��4��80%��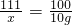 x=11.1g
x=11.1g =10%
=10%


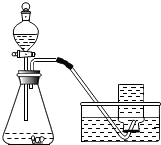 ij����С���о���Ӱ��H2O2 ����O2���������ء��Ŀ��⣮ͨ���������ϣ�����������²��룮
ij����С���о���Ӱ��H2O2 ����O2���������ء��Ŀ��⣮ͨ���������ϣ�����������²��룮 ij��ѧ��ȤС������ʦָ���£������ˡ�H2O2����O2�Ŀ�����ʲô�����йء���ʵ�飮��������ش��������⣮��ʵ�����20�������½��У�
ij��ѧ��ȤС������ʦָ���£������ˡ�H2O2����O2�Ŀ�����ʲô�����йء���ʵ�飮��������ش��������⣮��ʵ�����20�������½��У�