
【题目】学习二氧化碳性质时,将二氧化碳气体通入紫色石蕊溶液中,观察到紫色石蕊溶液变红,下列是某化学兴趣小组对紫色石蕊溶液变红色原因的实验探究。
(知识储备)浓硫酸可以吸收水分。
(提出问题)是什么物质使紫色石蕊变红色的?
(提出假设)①二氧化碳使紫色石蕊变为红色。②水使紫色石变为红色。③二氧化碳和水反应生成的碳酸使紫色石蕊变为红色。
(设计实验)
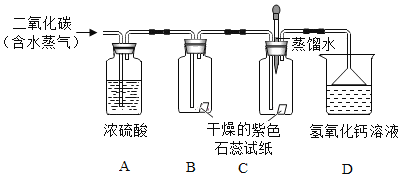
请根据他们的实验,回答下列问题
(1)装置A的作用是_____。
(2)实验过程中,B内试纸的颜色没有变化,这说明_____。
(3)C装置中未通入二氧化碳之前,在紫色石蕊试纸上滴入蒸馏水,未见试纸颜色变化,说明假设_____不成立(填序号,下同),之后通入二氧化碳,看到试纸变红,由此说明假设_____成立,原因是_____(用化学方程式填空)。
(4)D中反应的化学方程式为_____。
【答案】吸水干燥作用 二氧化碳不能使紫色石蕊变红色 ②; ③; CO2+H2O=H2CO3 CO2+Ca(OH)2=CaCO3↓+H2O
【解析】
(1)装置A的作用是:吸水干燥作用;故答案为:吸水干燥作用;
(2)实验过程中,B内试纸的颜色没有变化,这说明二氧化碳不能使紫色石蕊变红色;故答案为:二氧化碳不能使紫色石蕊变红色;
(3)C装置中未通入二氧化碳之前,在紫色石蕊试纸上滴入蒸馏水,未见试纸颜色变化,说明假设②不成立;之后通入二氧化碳,看到试纸变红,由此说明假设③成立,原因是二氧化碳和水反应生成碳酸,化学方程式为CO2+H2O=H2CO3,碳酸使紫色变红色;故答案为:②;③;CO2+H2O=H2CO3;
(4)二氧化碳会与氢氧化钙溶液反应生成碳酸钙沉淀和水;化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O。


科目:初中化学 来源: 题型:
【题目】模型是联系宏观与微观的桥梁。
(1)如图是钠原子结构示意图。

①X的数值为_________________。
②“11”指的是_________________。
③钠原子在化学反应中易失去1个电子,形成_______(填离子符号)。
(2)下图是氢分子和氧分子运动的示意图。

①在A、B和C中,能比较得出“温度越高,分子运动速率越快”的是__________(填标号)。
②从图中可见,影响分子运动速率的因素除温度外,还与______________________有关。
③举一个能说明“温度升高,分子运动速率加快”的生活事例:___________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】控制变量法是科学探究中常用的方法。化学反应的快慢常与外界条件有关,如温度、压强、催化剂、固体表面积等因素。以下实验设计的目的是探究化学反应快慢与外界条件的关系。
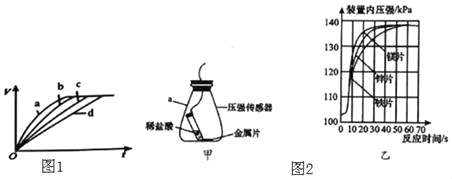
Ⅰ.现有四份等质量的铁分别与足量的盐酸进行反应,图1为随着反应时间的变化产生气体体积V的关系曲线。四组实验条件分别是:
a.50℃、铁粉 b.30℃、铁粉 c.30℃、铁丝 d.20℃、铁丝
(1)请写出铁与盐酸反应的化学方程式:_____,该反应进行时会放出热量。
(2)通过实验a和b对比,得出的结论是_____;若要比较金属铁的表面积对反应快慢的影响,应选择的实验组别是_____。实验中观察到产生气体“逐渐变快又变慢”,请解释“逐渐变快”的原因是_____。
Ⅱ.(3)常温时,用足量的铁、锌、镁三种金属片分别与等量盐酸反应,图2中,甲图为实验发生装置,乙图为测得的产生氢气的量(图中压强越大,表示产生氢气的量越多)。
①该实验中,你认为还需要控制的变量是_____;
②根据乙图,得出反应物的量与生成H2体积的关系是_____。
(4)若足量的镁片与盐酸反应,测得产生H2的实际值比理论值偏大,请分析可能的原因(写出一条即可):
_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CO在高温下还原Fe2O3的化学方程式为___________________;在该实验中常用澄清的石灰水检验反应生成的气体,其原理用化学方程式可表示为______________________;实验装置后端常放置一个燃着的酒精灯,其作用是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】星期日爸爸带小凯参观了科技馆,其中“物质之妙”展区蕴含着丰富的化学知识.

(1)A展示了金刚石的微观结构模型.构成金刚石的基本粒子是_____;
(2)B介绍了14C测年法.14C是质子数为6,中子数为8的碳原子,该原子中核外电子数为_____;
(3)C介绍了化学家门捷列夫及元素周期表.如图所示是元素周期表中某一周期元素的原子结构示意图:
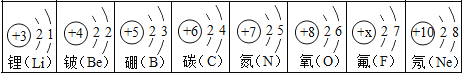
①表中氟原子的质子数X为_____,上述元素在周期表中位于同一周期的原因是_____;
②镁原子的结构示意图为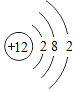 ,上图中与其化学性质相似的元素是_____;
,上图中与其化学性质相似的元素是_____;
③图中从左到右排列所遵循的一条变化规律是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“见著知微,见微知著”是化学的思维方法。

(1)从宏观知微观气体X在氧气中燃烧生成氮气和水,X分子中一定含有______原子。
(2)从微观知宏观:微粒A、B、C、D、E中,共有______种元素,元素的化学性质相似的是______,A和D组成化合物的化学式是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】世界上每年因锈蚀而报废的金属设备和材料,高达产量的20%~40%,某实验小组对铁的燃烧和锈蚀进行了如下探究。
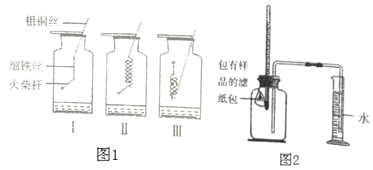
(探究一:铁丝燃烧)如图1所示,取三根粗细、长度均相同的光亮细铁丝,将其中两根盘成螺旋状。在每根铁丝一端系上一根粗铜丝,另一端系一根火柴杆。点燃火柴杆,待快燃尽时,分别插入盛有氧气的集气瓶中。观察到:Ⅰ和Ⅱ中的铁丝都剧烈燃烧,且Ⅱ中铁丝燃烧比I中更剧烈,Ⅲ中铁丝没有燃烧。
(1)集气瓶中装少量水的作用______。
(2)Ⅱ中铁丝燃烧比I中更剧烈的原因是______。
(3)Ⅲ中铁丝没有燃烧是因为______。
(探究二:铁粉腐蚀的条件)如图2所示,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内的水沿着导管慢慢进入广口瓶(容积为146mL)。当温度恢复到室温,量筒内水面高度不变时读数(此时广口瓶内氧气含量几乎为零),记录量筒内的起始和最终读数以及所需时间如下表:
序号 | 样品 | 量简起始读数 | 量简最后读数 | 所需时间 |
|
| 100 | 72 | 约120 |
| 10g铁粉、 | 100 | 72 | 约70 |
|
(4)金属锈蚀是金属与______发生了反应。
(5)实验①和②说明NaCl可以______(填“加快”或“减慢”)铁锈蚀的过程
(6)span>实验开始后,广口瓶温度升高,说明铁锈蚀是______(填“吸热”或“放热”)的过程。
(7)实验①和实验③是探究碳对铁锈蚀速率的影响,实验③表格的空白处样品的组成是______。
(8)该装置还可用于测量空气中氧气的含量,根据上述数据计算出空气中氧气的体积分数是______%(精确到小数点后一位),试分析实验结果出现误差的原因是______(写出一条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料与人类的生产和生活密切相关,请回答:
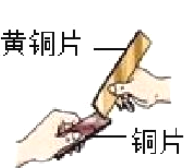
(1)铜片与黄铜片相互刻画,铜片表面留下明显划痕,说明铜片比黄铜片的硬度_______。(填“大”或“小”)
(2)不锈钢、黄铜(铜、锌合金)和碳化钨等是制作圆珠笔“笔头”的主要材料。下列关于这些材料的说法错误的是_______。
a.铁是不锈钢的主要组成元素之一
b.不锈钢与黄铜都具有耐腐蚀的性能
c.黄铜的导电性能比铜更好
d.碳化钨是一种混合物
(3)铜螺丝部位常出现一层绿色物质,这是由于铜生锈的原因,请完成该反应的化学方程:![]() _______
_______![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】仔细观察实验装置图,回答相关问题。
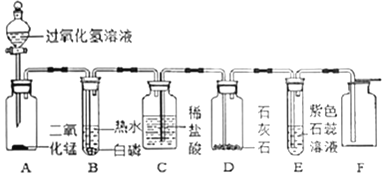
![]() 打开分液漏斗的活塞放出一定量过氧化氢溶液后,关上活塞,A中出现大量气泡,反应的化学方程式______。
打开分液漏斗的活塞放出一定量过氧化氢溶液后,关上活塞,A中出现大量气泡,反应的化学方程式______。
![]() 装置B中发生的现象说明燃烧的条件是______,反应的化学方程______。
装置B中发生的现象说明燃烧的条件是______,反应的化学方程______。
![]() 中液面下降,稀盐酸沿导管流入D瓶中,C中稀盐酸能流入D中的原因是______,写出D中反应的化学方程式______。
中液面下降,稀盐酸沿导管流入D瓶中,C中稀盐酸能流入D中的原因是______,写出D中反应的化学方程式______。
![]() 中紫色石蕊溶液变红的原因是______,反应的化学方程式______。
中紫色石蕊溶液变红的原因是______,反应的化学方程式______。
![]() 验证F装置气体收集满的方法是______。
验证F装置气体收集满的方法是______。
![]() 装置除用于实验室制取氧气外,还可用于氢气等气体的制取,用此装置制取气体的优点是______。
装置除用于实验室制取氧气外,还可用于氢气等气体的制取,用此装置制取气体的优点是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com