
| A. | Na2CO3溶液加入澄清石灰水中 | B. | Fe2O3加入稀盐酸中 | ||
| C. | 稀HCl滴入Ba(OH)2溶液中 | D. | CO2通入澄清石灰水中 |
分析 根据复分解反应发生的条件,若两种物质相互交换成分有沉淀、气体或水生成,则能发生化学反应,若没有沉淀、气体生成,则反应发生时现象不明显.
解答 解:A、Na2CO3溶液与澄清石灰水反应生成碳酸钙白色沉淀和氢氧化钠,能够发生化学反应,但有明显现象,故选项错误.
B、Fe2O3加入稀盐酸中生成硫酸铁和水,会观察到氢氧化铁溶解,溶液变黄,能够发生化学反应,但有明显现象,故选项错误.
C、稀HCl滴入Ba(OH)2溶液中,生成氯化钡和水,能够发生化学反应,且没有明显现象,故选项正确.
D、CO2通入澄清石灰水生成碳酸钙沉淀和水,会观察到澄清的石灰水变浑浊,故选项错误.
故选:C.
点评 本题难度不大,考查同学们利用复分解反应发生的条件能否发生化学反应,解题时还要注意没有明显现象这一限制条件.


科目:初中化学 来源: 题型:选择题
| A. | 因为干冰易升华,升华时吸收大量的热,所以可用于人工降雨 | |
| B. | 蚊虫叮咬后,会在人的皮肤内分泌蚁酸使皮肤肿痛,可涂醋酸来减轻痛痒 | |
| C. | 因为氮气化学性质不活泼,所以氮气可用于食品防腐 | |
| D. | 甲醛能使蛋白质变性起到防腐作用,所以甲醛水溶液可用于浸泡标本 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
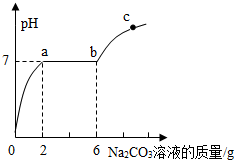 某实验小组的同学用氢氧化钡溶液与稀盐酸进行中和反应,结束后取10g反应后溶液逐滴滴入质量分数为13.25%碳酸钠溶液,测得溶液PH与加入的碳酸钠溶液的质量关系如图所示,则下列说法正确的是( )
某实验小组的同学用氢氧化钡溶液与稀盐酸进行中和反应,结束后取10g反应后溶液逐滴滴入质量分数为13.25%碳酸钠溶液,测得溶液PH与加入的碳酸钠溶液的质量关系如图所示,则下列说法正确的是( )| A. | 中和反应时氢氧化钡溶液与稀盐酸恰好完全反应 | |
| B. | 图中oa段反应为BaCl2+Na2CO3═BaCO3↓+2NaCl | |
| C. | 图中c点溶液中的溶质有2种 | |
| D. | 图中b点产生的沉淀质量是0.985g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 事实 | 解释 |
| A | 在花园中可闻到花香 | 分子在不断运动 |
| B | 用肉眼不能直接观察到CO2分子 | CO2分子很小 |
| C | 50毫升水与50毫升乙醇混合,混合后总体积小于100毫升 | 分子之间有间隔 |
| D | 冰受热变为水,水受热变为水蒸气 | 分子可以再分 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
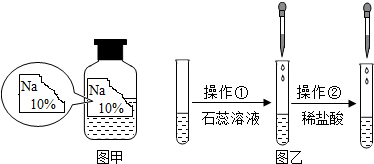 某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.
某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
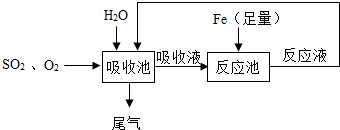 某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.
某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com