
| ��Ӧǰ���ʵ�����/g | ��Ӧ�����ʵ�����/g | |
| Cu-Zn�Ͻ� | ϡ���� | ��Һ |
| 4.0 | 10 | 11.89 |
���� ��1�����ݺϽ����ڽ������Ͻ��з�����
��2������Cu-Zn�Ͻ��ĩ�ŵ�ʢ��10gϡ������ձ��У�ǡ����ȫ��Ӧ���з�����
��3������п�����ᷴӦ��������п����������������������������п��������
��4���������������Һ������������п���з�����
��� �⣺��1��Cu-Zn�Ͻ����ڽ������ϣ�
��2��Cu-Zn�Ͻ��ĩ�ŵ�ʢ��10gϡ������ձ��У�ǡ����ȫ��Ӧ�����Թ������õ���Һ�е����ʻ�ѧʽΪZnSO4��
��3����������������x+10g-11.89g=x-1.89g��
��ͭп�Ͻ���Zn����Ϊx����������п������Ϊy��
Zn+H2SO4=ZnSO4+H2��
65 161 2
x y x-1.89g
$\frac{65}{x}$=$\frac{2}{x-1.89g}$
x=1.95g
$\frac{65}{1.95g}$=$\frac{161}{y}$
y=4.83g
��4�����������Һ��������������Ϊ��$\frac{4.83g}{11.89g}$��100%=40.6%��
�ʴ�Ϊ����1��������
��2��ZnSO4��
��3��ԭCu-Zn�Ͻ���Zn������Ϊ1.95g��
��4�����������Һ��������������Ϊ��40.6%��
���� �ڽ������ʱ��Ҫ������֮��Ĺ�ϵ���ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
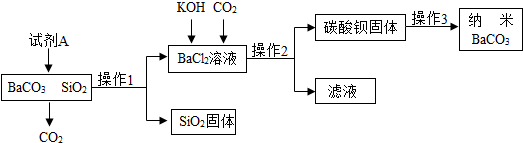
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ո��ۺ����� | |
| B�� | Ұ����չ�ҵ���� | |
| C�� | �۸��̴��ŷ��̳� | |
| D�� | Ϊ�˼���������������ֹʹ��˽�ҳ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Լռ������������21%��Ŀǰ������Ⱦָ������Ŀ��pM2.5�������� | |
| B�� | �����к�������Ԫ�������������õ�½�ص�ˮֻԼռȫ��ˮ������2.53% | |
| C�� | ���ܵ����ÿ��Լ�������ЧӦ��ʯ�Ϳ����Ƴ����͡�ú�ͺ����͵Ȳ�Ʒ | |
| D�� | ��˿���۵���ߵĽ������Ƴɣ��Ͻ��ǿ�Ⱥ�Ӳ��һ����������Ĵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KC1��KC1O3��--�Ӷ������̣����Ⱥ���ȴ | |
| B�� | N2��O2��--ͨ�����ȵ�ͭ�� | |
| C�� | CO2��CO��--ͨ������������������Һ | |
| D�� | KCl��Һ��CaC12��Һ��--�μ�̼������Һ��ǡ����ȫ��Ӧ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 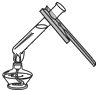 ����Һ�� | B�� | 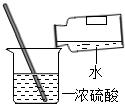 ϡ��Ũ���� | C�� | 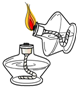 ��ȼ�ƾ��� | D�� |  ��������ζ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
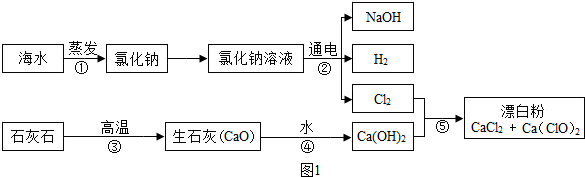
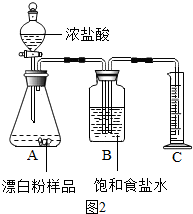
| ʵ����� | ʵ������ | ʵ����� |
| ��ȡ������Ʒ���Թ��У��μ�������ϡ���ᣮ | ���������������ʹʯ��ˮ����ǣ� | ����2���� |
| ����������Ӧ����Թ��м�����Ʒ����Һ�� | ��ɫ��dz����ʧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ���ڻ����ó涣ҧ���ʹ����----����ˮ�������� | |
| B�� | ����������������----�����µ�����ѧ�����ȶ� | |
| C�� | ϴ�ྫ��ϴ������----ϴ�ྫ���ܽ����� | |
| D�� | ϡ���������----ϡ�����������ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢۢ� | B�� | �ڢ٢� | C�� | �ۢڢ� | D�� | �ۢ٢� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com