
【题目】CaCO3在生产生活中有广泛的用途。
(1)煅烧石灰石可制得活性CaO,反应的化学方程式为_______。为测定不同 煅烧温度对CaO活性的影响,取石灰石样品分为三等分,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时 间的变化如图1所示.可知:CaO与水反应会_______热量(填“放出”或“吸收”);上述温度中,______℃煅烧所得 CaO 活性最高.要得出正确结论,煅烧时还需控制的条件是_________。
(2)以电石渣[主要成分为 Ca(OH)2,还含有少量 MgO 等杂质]为原料制备高纯 CaCO3的流程如下:
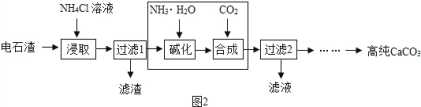
①如图为 NH4Cl 浓度对钙、镁浸出率的响(![]() )。可知:较适宜的 NH4Cl溶液的质量分数为______;浸取时主要反应的化学方程式为_______。
)。可知:较适宜的 NH4Cl溶液的质量分数为______;浸取时主要反应的化学方程式为_______。
②流程中大方框内部分若改用___溶液(填化学式),可一步得到与原流程完全 相同的生成物。
③该流程中可循环利用的物质有________。
【答案】CaCO3![]() CaO+CO2↑ 放出 900 煅烧时间相同 10% 2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑ (NH4)2CO3 NH4Cl(NH3)
CaO+CO2↑ 放出 900 煅烧时间相同 10% 2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑ (NH4)2CO3 NH4Cl(NH3)
【解析】
(1)煅烧石灰石可制得活性CaO,反应原理是碳酸钙高温条件下反应生成氧化钙和二氧化碳,化学方程式为CaCO3![]() CaO+CO2↑。为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等分,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如图1所示.可知:CaO与水反应会放出热量;由图中信息可知,上述温度中,900℃煅烧所得 CaO 活性最高.要得出正确结论,煅烧时还需控制的条件是煅烧时间相同;
CaO+CO2↑。为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等分,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如图1所示.可知:CaO与水反应会放出热量;由图中信息可知,上述温度中,900℃煅烧所得 CaO 活性最高.要得出正确结论,煅烧时还需控制的条件是煅烧时间相同;
(2) ①通过分析图象中氯化铵浸出钙离子的质量分数可知,较适宜的NH4Cl溶液的质量分数为10%,氯化铵和氢氧化钙反应生成氯化钙、氨气和水,所以浸取时主要反应的化学方程式为:2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O;
②图中的流程分析可知,氨水、水、二氧化碳反应生成碳酸氢铵,故氨水、水、二氧化碳和碳酸氢铵所起的作用是相同的,所以流程中虚线内部分若改用NH4HCO3溶液;
③除了氨气可以循环使用,NH4Cl可以循环使用。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:初中化学 来源: 题型:
【题目】实验室用如图所示装置的部分或全部组合后完成如下实验,请回答下列问题:
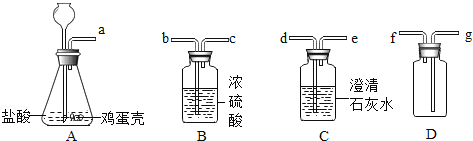
(1)若要证明鸡蛋壳的主要成分是碳酸盐如碳酸钙,将A装置中的导气管a与C装置中的导气管d相连,当装置C中产生______的现象时即达到实验目的。
(2)若将A装置中的药品换成稀硫酸和锌粒,发生反应的化学方程式为______,该反应的基本类型为______。若需要将产生的氢气经干燥后,再用D装置收集,当D装置的瓶口向下时,导管口的连接顺序应该是:a→b→c→______(选填“f”或“g”)。
(3)用烧杯稀释浓硫酸时,应向烧杯中倒入的物质是______。B装置中使用过的浓硫酸经稀释后形成稀硫酸,例举稀硫酸的一种具体用途为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
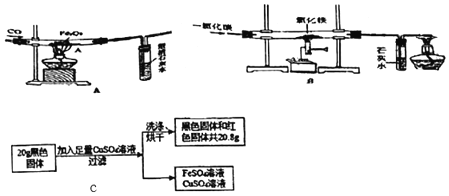
【题目】杨敏在实验室进行CO还原氧化铁的实验采用酒精灯加热(图A)与书本实验(图B)现象相同,发现在得到的黑色粉末中加稀盐酸,没有气泡产生,杨敏就图A实验中反应后得到的黑色粉末的成分进行了如下探究。
(查阅资料)①铁粉及铁的几种常见氧化物的颜色及部分性质。
物质 | 铁粉 | Fe2O3 | Fe3O4 | FeO |
颜色 | 黑色 | 红棕色 | 黑色 | 黑色 |
能否被磁铁吸引 | 能 | 不能 | 能 | 不能 |
②实验室酒精灯的温度为400﹣500℃,酒精喷灯的加热温度在1000℃左右。
③当温度高于300℃以上,Fe2O3容易被还原成Fe3O4;当温度高于600℃以上,Fe3O4容易被还原FeO;当温度高于700℃以上,FeO容易被还原成Fe;
(提出问题)图A实验得到黑色粉末的成分是什么?
(提出猜想)黑色粉末的成分是:①FeO、Fe3O4②FeO③Fe3O4;④FeO、Fe3O4、Fe2O3。
(分析与评价)猜想_____错误,理由是_____。
(1)装置A有一处明显错误,该错误是_____。
(2)请写出澄清石灰水中发生的反应的化学方程式_____。
(3)由对比实验可知,还原氧化铁的实验产物与_____有关。
(实验设计)将图A实验得到黑色粉末倒在一表面皿中,用磁铁接触黑色粉末,出现_____现象,说明猜想②正确。
(4)实验B最后得到的黑色固体可能是Fe和Fe3O4,中的一种或两种。小海设计如下实验探究其成分,请帮助他完成该探究过程。
(探究过程)①定性研究:取少量的图B实验得到的黑色粉末于一试管中,加入适量的硫酸铜溶液,充分振荡,出现_____现象,证明黑色固体中有铁。
②定量研究:取B实验得到的黑色固体20g,设计如图C实验:试推测黑色固体的成分是_____。
③有同学试图通过反应前后固体质量的变化来确定黑色固体的成分,你认为可行吗?(假设氧化铁在反应中完全反应)_____(填“行”或“不行”)理由是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如下表所示:
加入稀盐酸的质量/g | 生成气体的总质量/g | |
第1次 | 20 | 1.1 |
第2次 | 20 | 2.2 |
第3次 | 20 | m |
第4次 | 20 | 4.4 |
第5次 | 20 | 4.4 |
(1)m的值为_________g
(2)12g石灰石样品中碳酸钙的质量等于_________g
(3)反应完全后最终溶液中氯化钙的质量分数为_______?(写出计算过程,计算结果精确至0.1)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种物质的溶解度曲线,回答下列问题:
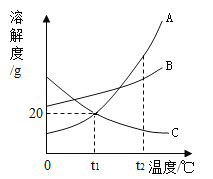
(1)在t1℃时,将30gA物质加入到50g水中所得溶液的质量为_______g;
(2)A中混有少量B,提纯A的方法是_______;
(3)将t2℃时A、B、C的饱和溶液降温至t1℃。此温度下A、B、C的溶液的溶质质量分数由小到大的顺序__(用“<”连接)
查看答案和解析>>
科目:初中化学 来源: 题型:
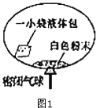
【题目】某研究小组对自动充气气球(如图1)进行下探究。
(查阅资料)
①该气球的充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧 化碳气体,实现气球自动充气。
②氯化钙水溶液呈中性,碳酸钠、碳酸氢钠的水溶液均呈碱性。
③用一定溶质质量分数的 NaHCO3和Na2CO3溶液进行实验,实验现象记录如下:
NaHCO3溶液 | Na2CO3溶液 | |
加入澄清石灰水 | 溶液变浑浊 | 溶液变浑浊 |
加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 |
加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
探究1:气体的成分
为检验气体是二氧化碳,可选用______(填试剂名称).
探究2:液体包内溶液的酸碱性
室温时,用 pH试纸测得溶液的 pH 的方法是____;若 测得溶液的 pH=3,则该溶液呈___性。
探究 3:白色粉末的成分
(猜想与假设)甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠;丁同学 认为是碳酸钠和碳酸氢钠的混合物。
(进行实验)
(1)将少量白色粉末放入水中搅拌,观察到______,说明甲同学的猜想不正确。
(2)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的
10%的盐酸(装置如图2),记录如下表:


(解释与结论)
(1)实验Ⅰ的化学方程式为__________。
(2)表中a=_______;V1________V2(填“>”、“<”或“=”)。
(3)上述实验得出的结论及判断依据是__________。
(反思与评价)老师指出还可以采用更简单的方法得出与上述实验(2)相同的结论,实验方案为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合如图所示实验,回答下列问题。

(1)实验一的目的是利用浓氨水的碱性和挥发性,验证______。
(2)实验二中,在B试管加入______(写出一种情况),即可证明温度和固体颗粒大小都是影响冰糖溶解快慢的因素。
(3)实验三中,通过测定水和氯化钠混合前后的质量不能用来验证质量守恒定律,原因是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙可以合成清洁燃料丙,微观过程如图。下列说法错误的是
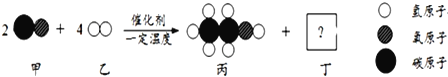
A. 丁的化学式为H2O B. 丙中C、H、O的质量比为12:3:8
C. 该反应中有三种氧化物 D. 参加反应的甲和乙的质量比是7:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图回答下列问题:

(1)写出图中仪器①的名称_________.
(2)实验室准备用氯酸钾制取比较纯净的氧气,采用的装置组合是_________,该反应的化学方程式为____________.
(3)实验室制取二氧化碳的化学方程式为_________,收集装置______,如何验满? _______
(4)氨气是无色、有刺激性气味、极易溶于水的气体,实验室常用加热氯化铵和熟石灰固体混合物的方法制取氨气,则实验室制取并收集氨气的最佳装置组合是_____.(填字母)
(5)某化学兴趣小组进行如下组合实验,对二氧化碳的性质进行验证。

当打开A装置中的分液漏斗活塞后,回答下列问题。
①A中发生反应的化学方程式为_________。
②B中白磷能够燃烧的原因是____________。
③G烧杯中现象说明二氧化碳具有的物理性质是__________ 。
④E处使紫色石蕊变成红色的物质的化学式_________;写出F处发生变化的化学方程式________
(6)小海用如图G装置验证二氧化碳与水的反应,为说明使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是_______(填序号,可重复选用).
①从b端通氮气 ②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
③从a端通二氧化碳 ④从分液漏斗中滴加适量水.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com