
| 实验 | 实验步骤 | 实验现象 |
| ① | 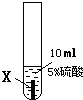 |
X片表面无明显变化 |
| ② | 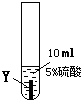 |
Y片表面无明显变化 |
| ③ | 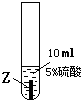 |
Z片溶解,表面有无色氢气产生,溶液最终为无色 |
| 实验 | 实验步骤 | 实验现象 |
| ④ | 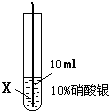 |
在X丝表面有银白色的固体析出 |
| ⑤ | 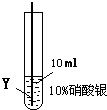 |
在Y丝表面没有明显现象 |
| 实验编号 | 硫酸的质量分数/% | 反应的温度 | Z丝消失的时间/S |
| ⑥ | 3 | 20 | 500 |
| ⑦ | 6 | 20 | 300 |
| ⑧ | 6 | 30 | 80 |


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:初中化学 来源: 题型:阅读理解

| 编号 | 实验I | 实验II | 实验III |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
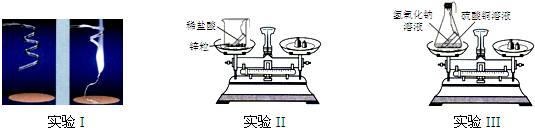
| 编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com