含钠元素、钙元素的化合物是初中化学的重要研究对象之一.
(一)某学习小组的同学在学习了Na
2CO
3、NaHCO
3的性质后,了解到它们都能与盐酸反应产生CO
2气体,那么如何鉴别Na
2CO
3和NaHCO
3呢?带着这样的疑问,他们进行了下列探究:
【查阅资料】(1)Ca(HCO
3)
2可溶于水;
(2)NaHCO
3固体受热分解生成碳酸钠、二氧化碳和水.
【猜想】(1)甲同学认为可用澄清石灰水鉴别Na
2CO
3和NaHCO
3溶液.
(2)乙同学认为可用CaCl
2溶液鉴别Na
2CO
3和NaHCO
3溶液.
甲、乙两同学的猜想是依据澄清石灰水、CaCl
2溶液分别与Na
2CO
3溶液反应均有沉淀产生;又知道Ca(HCO
3)
2可溶于水,因此猜测澄清石灰水、CaCl
2溶液分别与NaHCO
3溶液混合不会产生沉淀,从而鉴别出两种溶液.
(3)丙同学认为固体Na
2CO
3、NaHCO
3可用加热的方法鉴别.
【实验探究】(1)甲同学在两支分别盛有少量Na
2CO
3、NaHCO
3溶液的试管中,各加入澄清石灰水,观察到两支试管中的现象相同,均产生了白色沉淀,实验结果与猜想不一致,即不能用澄清石灰水鉴别Na
2CO
3和NaHCO
3溶液.
(2)乙同学将CaCl
2溶液加入到分别盛有少量Na
2CO
3、NaHCO
3溶液的试管中,发现两支试管中也都产生了白色沉淀,实验结果出乎意料,但根据观察到的其他实验现象,他认为仍可用CaCl
2溶液鉴别Na
2CO
3和NaHCO
3溶液.
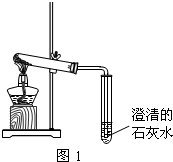
(3)丙同学分别取了一定量的Na
2CO
3、NaHCO
3固体于大试管中加热(如图1):
①加热Na
2CO
3时,开始即见小试管中有少量气泡产生,继续加热,气泡逐渐减少,未见澄清石灰水变浑浊,
②加热NaHCO
3时,丙同学观察到实验现象与①不同,证实了自己的猜想是合理的.
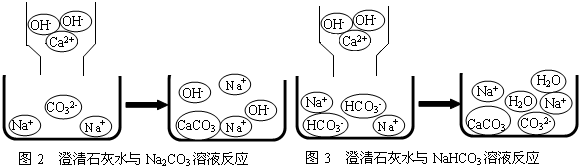
【问题讨论】(1)小组同学对上述实验展开了讨论,对甲同学的两个实验进行了比较,并从物质在溶液中解离出不同离子的微观角度分析了原因(如图2、图3).请写出Na
2CO
3与澄清石灰水发生反应的化学方程式
;写出NaHCO
3与澄清石灰水混合时参与反应的离子:
.
(2)乙同学的两个实验中,大家对CaCl
2与Na
2CO
3溶液的反应比较熟悉,而对CaCl
2与NaHCO
3溶液混合产生的现象难以理解,同学们又进一步查阅了资料,了解到CaCl
2与NaHCO
3溶液可发生如下反应:CaCl
2+2NaHCO
3=CaCO
3↓+2NaCl+CO
2↑+H
2O,因而同学们知道了乙同学是通过观察到
现象来鉴别Na
2CO
3和NaHCO
3溶液的.至于CaCl
2与NaHCO
3溶液为什么能发生上述反应,老师指出其反应原理较复杂,有待于今后学习中进一步探究.
(3)丙同学在加热Na
2CO
3固体时,开始产生少量气泡的原因是
;根据你分析:Na
2CO
3受热
分解(填“易”或“不易”).在加热NaHCO
3固体时,丙同学观察到的实验现象是
(任写一种).
【拓展应用】(1)固体Na
2CO
3中混有少量NaHCO
3,可通过
方法除去.
(2)要除去Na
2CO
3溶液中混有的少量NaHCO
3,可加入适量的
溶液.
(二)实验室里同学们正在进行探究实验.用A、B、C、D四支试管各取室温下等体积的氢氧化钙饱和溶液,再向A试管中滴加碳酸钠溶液、B试管中滴加氯化铜溶液、C试管中滴加氯化铵溶液、D试管中滴加氯化钠溶液,振荡.
【提出问题】:他们在探究的问题是氢氧化钙能否与
(选填“酸”、“碱”、“盐”)发生反应?
【表达与交流】:①阳阳同学根据在D试管中没有看到明显现象,判断D试管中无化学反应发生.你认为此判断的依据是否合理
(填“合理”或“不合理”),并解释其原因是
;
②为科学处理实验过程中产生的废液,同学们对B试管中反应后过滤得到的无色滤液,继续进行探究.阳阳同学猜想滤液中只含有一种溶质,娇娇同学猜想滤液中含有两种溶质.为验证哪位同学的猜想是正确的,同学们选用两种不同类别的物质进行以下两个实验.请填写下列实验报告:
| 实验内容 |
实验现象 |
实验结论 |
| 方案一:取少量滤液加入试 管中,向其中 |
|
娇娇同学的猜想是正确的.
滤液中含有的两种溶质是
|
| 方案二:取少量滤液加入试管中,向其中 |
|
【反思与评价】:通过上述实验,同
学们认为实验过程中产生的废液必须处理后再排放.请你对B试管中滤液的处理提出可行的建议
(三)现有CaCO
3 和KHCO
3的混合物,甲、乙两同学分别称取一定质量的该混合物来判定其中两种成分的质量比.
①甲同学称取2.00g混合物,向其中加入过量的盐酸,生成气体的质量为ag,则a=
.该同学能否由气体质量计算出混合物中两成分的质量比?
(填“能”或“不能”)
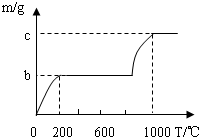
②已知KHCO
3 和NaHCO
3一样加热易分解,K
2CO
3的分解温度远高于1000℃.乙同学称取Wg混合物充分加热,所得CO
2气体质量(m) 随温度(T)变化的曲线如图所示,则m(CaCO
3):m(KHCO
3)═
(用含b、c的代数式表示)

 阅读快车系列答案
阅读快车系列答案 含钠元素、钙元素的化合物是初中化学的重要研究对象之一.
含钠元素、钙元素的化合物是初中化学的重要研究对象之一.
 学们认为实验过程中产生的废液必须处理后再排放.请你对B试管中滤液的处理提出可行的建议
学们认为实验过程中产生的废液必须处理后再排放.请你对B试管中滤液的处理提出可行的建议

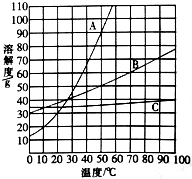 A、B、C三种固体物质溶解度随温度变化的曲线如图所示,请回答下列问题:
A、B、C三种固体物质溶解度随温度变化的曲线如图所示,请回答下列问题:
 A、B、C三种固体物质溶解度随温度变化的曲线如图所示,请回答下列问题:
A、B、C三种固体物质溶解度随温度变化的曲线如图所示,请回答下列问题: