


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
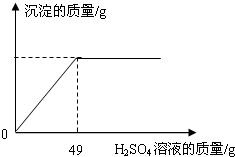
| 硫酸(500mL) 品名 硫酸 化学式 H2SO4 相对分子质量98 密度 1.84g/cm3 质量分数98%(1)该试剂瓶中硫酸溶液的质量是 (2)某固体物质由氯化钠和氯化钡组成,取32.8g该固体混合物完全溶于水,并逐滴加入上述20%的稀硫酸,产生沉淀的质量与加入稀硫酸的质量有如图所示关系,计算32.8g固体混合物中氯化钠和氯化钡的质量.(H2SO4+BaCl2═BaSO4↓+2HCl) 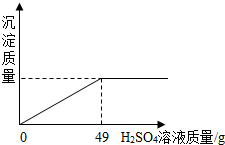
查看答案和解析>> 科目:初中化学 来源: 题型: 实验室现有碳酸钠和氯化钠的固体混合物样品.小炜同学想测定样品中碳酸钠的质量分数,先称取该混合物样品20g,完全溶于水中,然后取用了一定溶质质量分数的氯化钙溶液80g平均分4次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:?
1.5 1.5 g;?(2)计算原固体混合物样品中碳酸钠的质量分数是多少? 查看答案和解析>> 科目:初中化学 来源: 题型:阅读理解 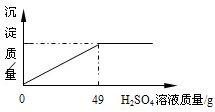 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算: 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算:
|