
2.3 g某物质在空气中完全燃烧,生成4.4 g二氧化碳和
2.7 g水,则该物质中一定含有_______ _元素(填元素符号),其质量比为________。
_元素(填元素符号),其质量比为________。
【解析】本题考查质量守恒定律的应用。由质量守恒定律知参加反应氧气的质量为4.4 g+2.7 g-2.3 g=4.8 g,4.4 g二氧化碳中碳元素、氧元素的质量分别为4.4 g×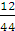 ×100%=1.2 g、4.4 g×
×100%=1.2 g、4.4 g× ×100%=3.2 g,2.7 g水中氢元素、氧元素的质量分别为0.3 g、2.4 g,生成物中氧元素的质量总和为3.2 g+2.4 g=
×100%=3.2 g,2.7 g水中氢元素、氧元素的质量分别为0.3 g、2.4 g,生成物中氧元素的质量总和为3.2 g+2.4 g=
5.6 g>4.8 g,所以该物质中一定含有碳、氢、氧元素。碳元素的质量为1.2 g,氢元素的质量为0.3 g,氧元素的质量为5.6 g-4.8 g=0.8 g,所以碳、氢、氧元素的质量比为12∶3∶8。
答案:C、H、O 12∶3∶8
【方法归纳】燃烧法判断物质所含元素的种类
(1)碳、氢元素的判断:物质在空气中燃烧,若有二氧化碳和水生成,根据质量守恒定律可以判断,该物质含碳元素和氢元素,因为碳、氢元素对应的生成物分别为C→CO2,H→H2O。
(2)氧元素的判断:由于物质在空气中燃烧,氧气参与了反应,故该物质是否含氧元素无法判断 ,可以根据反应的氧气的质量与生成物中氧元素的质量和进行比较。若反应的氧气的质量等于生成物中氧元素的质量之和,则该物质不含氧元素;若小于生成物中氧元素的质量之和,则该物质含氧元素。
,可以根据反应的氧气的质量与生成物中氧元素的质量和进行比较。若反应的氧气的质量等于生成物中氧元素的质量之和,则该物质不含氧元素;若小于生成物中氧元素的质量之和,则该物质含氧元素。


科目:初中化学 来源: 题型:
右图是甲、乙两种粒子的结构示意图,下列有关 说法正确的是( )
说法正确的是( )
A.甲粒子的化学性质比乙粒子稳定
B.两种粒子属于同种元素
|
查看答案和解析>>
科目:初中化学 来源: 题型:
下列实验现象描述不正确的是 ( )
A. 红磷在空气中燃烧产生大量白烟 B. 硫在氧气中燃烧产生淡蓝色火焰
C. 铁丝在氧气中剧烈燃烧,火星四射 D. 木炭在空气中燃烧发出红光
查看答案和解析>>
科目:初中化学 来源: 题型:
下表是元素周期表的一部分,据此回答下列问题。
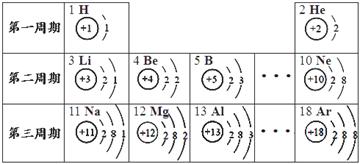
(1)表中12号元素的名称是 ,该元素的原子在化学反应中易 (填“得到”或“失去”)电子,形成离子,其离子符号是 。
(2)从原子结构入手,找出第三周期元素为什么处于同周期______________。
(3)原子序数为8和13的两种元素组成的化合物是 (写化学式)
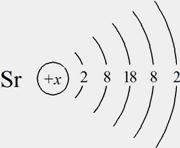
(4)右上图是元素锶(Sr)的原子结构示意图,则x= ,锶元素的氧化物的化学式为 。通过上表分析可知,锶元素位于元素周期表第 周期。
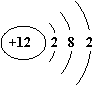
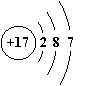 (5)下列与锶元素化学性质相似的是 (填字母)。
(5)下列与锶元素化学性质相似的是 (填字母)。
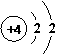
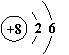
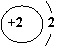
A B C D E
查看答案和解析>>
科目:初中化学 来源: 题型:
下图为某反应的微观示意 图,“
图,“ ”和“
”和“ ”表示两种不同的原子,下列说法正确的是 ( )
”表示两种不同的原子,下列说法正确的是 ( )
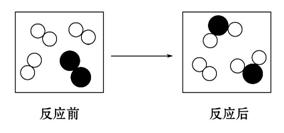
A.反应前后原子数目不变
B.反应中有单质生成
C.反应前后分子种类不变
D.参加反 应的两种分子个数比为3∶1
应的两种分子个数比为3∶1
查看答案和解析>>
科目:初中化学 来源: 题型:
小军根据燃烧红磷测定空气中氧气含量的实验原理,认为可用木条燃烧产生的木炭代替红磷测定空气中氧气的含量,并按如图装置进行实验.
①依据的实验原理是 .
②小军检查装置气密性后,将盛有足量红热木炭的燃烧匙迅速伸入集气瓶中,并把塞子塞紧,待红热的木炭熄灭并冷却至室温后,打开弹簧夹,并未发现倒吸现象.经过认真分析,小军发现实验失败的原因是(答一条) .
③小军反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是(答一条) .

查看答案和解析>>
科目:初中化学 来源: 题型:
铝在氧气中燃烧可生成氧化铝。在该反应中,铝、氧气、氧化铝的质量比是
( )
A.27∶32∶102 B.27∶24∶43
C.4∶3∶2  D.108∶96∶204
D.108∶96∶204
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com