
| A£® | ¢Ł¢Ś | B£® | ¢Ū¢Ü | C£® | ¢Ś¢Ū | D£® | ¢Ł¢Ü |
·ÖĪö ¢Łøł¾ŻÖŹĮæŹŲŗć¶ØĀÉ£¬·“Ó¦Ē°ŗóŌŖĖŲµÄÖÖĄą²»±ä£¬øł¾Ż¼ĘĖ涞Ńõ»ÆĢ¼ÖŠµÄĢ¼ŌŖĖŲµÄÖŹĮæŗĶøł¾Ż»Æѧ·½³ĢŹ½¼ĘĖć£¬Ė®µÄÖŹĮæ¼°ĘäĒāŌŖĖŲµÄÖŹĮæ£¬Č·¶ØĪļÖŹµÄ×é³É£»
¢ŚÓÉ8.8gCO2£¬æɼĘĖć³öĢ¼ŌŖĖŲµÄÖŹĮ棬ŌŁ¼ĘĖćRÖŠĢ¼ŌŖĖŲµÄÖŹĮæ·ÖŹż£»
¢Ūøł¾Ż»Æѧ·½³ĢŹ½¼ĘĖć£¬ŅŃÖŖ6.4gijĪļÖŹRĶźČ«Č¼ÉÕÉś³É8.8gCO2£¬æɼĘĖćÉś³ÉµÄĖ®µÄÖŹĮ棻
¢Üøł¾Ż»Æѧ·½³ĢŹ½¼ĘĖć£¬ŅŃÖŖ6.4gijĪļÖŹRĶźČ«Č¼ÉÕÉś³É8.8gCO2£¬æɼĘĖćRµÄĻą¶Ō·Ö×ÓÖŹĮ森
½ā“š ½ā£ŗ¢Łøł¾ŻÖŹĮæŹŲŗć¶ØĀÉ£¬·“Ó¦Ē°ŗóŌŖĖŲµÄÖÖĄą²»±ä£ŗ8.8g”Į$\frac{12}{44}$”Į100%=2.4g£»
øł¾Ż»Æѧ·½³ĢŹ½¼ĘĖć£¬ÉčĖ®ÖŹĮæĪŖx£¬
2R+3O2$\frac{\underline{\;µćČ¼\;}}{\;}$2CO2+4H2O
88 72
8.8g x
Ōņ$\frac{88}{72}=\frac{8.8g}{x}$
x=7.2g
¹ŹĒāŌŖĖŲµÄÖŹĮæĪŖ7.2g”Į$\frac{2}{18}$”Į100%=0.8g£»
Ģ¼ŌŖĖŲµÄÖŹĮæ+ĒāŌŖĖŲµÄÖŹĮæ=2.4+0.8£¼6.4£¬¹ŹRÓ¦ÓÉĢ¼”¢Ēā”¢ŃõŌŖĖŲČżÖÖŌŖĖŲ×é³É£»¹Ź¢Ł“ķĪó£»
¢ŚÓÉ8.8gCO2£¬æɼĘĖć³öĢ¼ŌŖĖŲµÄÖŹĮæĪŖ£ŗ8.8g”Į$\frac{12}{44}$”Į100%=2.4g£¬ŌŁ¼ĘĖćRÖŠĢ¼ŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ£ŗ$\frac{2.4g}{6.4g}$”Į100%=37.5%£»¹Ź¢ŚÕżČ·
¢Ūøł¾Ż¢ŚÖŠ¼ĘĖć£¬¹Ź¢Ū6.4gRČ¼ÉÕ»¹Éś³ÉĮĖ7.2gH2O£¬ÕżČ·£»
¢Üøł¾Ż»Æѧ·½³ĢŹ½¼ĘĖć£¬ÉčRµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖy£¬
2R+3O2$\frac{\underline{\;µćČ¼\;}}{\;}$2CO2+4H2O
2R 88
6.4g 8.8g
$\frac{2R}{88}=\frac{6.4g}{8.8g}$
½āµĆR=32£®¹Ź¢ÜRµÄĻą¶Ō·Ö×ÓÖŹĮæµČÓŚ64£¬“ķĪó
¹ŹŃ”C£®
µćĘĄ ŅŖĒóÕĘĪÕ²¢Ąķ½āø÷ŌŖĖŲµÄĻą¶ŌŌ×ÓÖŹĮæµÄ×÷ÓĆ£»ĒóĪļÖŹÖŠø÷ŌŖĖŲµÄ±ČÖµ£¬¼ĘĖćij·Ö×ÓµÄĻą¶Ō·Ö×ÓÖŹĮ棬ĒóijĪļÖŹÖŠÄ³ŌŖĖŲµÄÖŹĮæ·ÖŹż¶¼ŹĒ»ł±¾µÄ¼ĘĖć£®


 ³¤½×÷Ņµ±¾Ķ¬²½Į·Ļ°²įĻµĮŠ“š°ø
³¤½×÷Ņµ±¾Ķ¬²½Į·Ļ°²įĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĆĢ Mn | B£® | ĀĮ AL | C£® | øĘ cA | D£® | ÄÉ Na |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
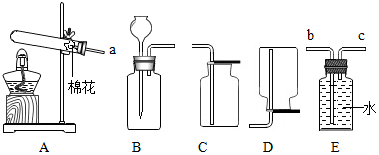 ŹµŃé²Ł×÷æ¼ŹŌÖŠĪŖĮĖÖĘČ”ŃõĘųŗĶ¶žŃõ»ÆĢ¼£¬ŹµŃéŹŅĢį¹©ĮĖŅŌĻĀŅ©Ę·ŗĶŅĒĘ÷×°ÖĆ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ŹµŃé²Ł×÷æ¼ŹŌÖŠĪŖĮĖÖĘČ”ŃõĘųŗĶ¶žŃõ»ÆĢ¼£¬ŹµŃéŹŅĢį¹©ĮĖŅŌĻĀŅ©Ę·ŗĶŅĒĘ÷×°ÖĆ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2 H2CO3 | B£® | CO2 CaCO3 | C£® | CO2 Ca£ØOH£©2 | D£® | CO CO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
| ŹµŃé×°ÖĆ | ŹµŃé²½Öč | ·ÖĪö |
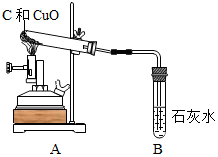 | ¢Ł¼ģŃé×°ÖĆĘųĆÜŠŌ | |
| ¢Ś°ŃľĢæŗĶŃõ»ÆĶµÄ»ģŗĻĪļ·ÅČėŹŌ¹Ü£¬Čē×óĶ¼ĖłŹ¾Į¬½ÓŹµŃé×°ÖĆ | ×°ÖĆÖŠ“ęŌŚµÄĪŹĢāŹĒBŹŌ¹Ü“¦²»Ó¦øĆÓŠĻšĘ¤Čū£» | |
| ¢ŪøĽų×°ÖĆŗ󣬵ćČ¼¾Ę¾«ÅēµĘæŖŹ¼ŹµŃé | ×°ÖĆBµÄ×÷ÓĆŹĒ¼ģŃé²śĪļŹĒ·ńÓŠ¶žŃõ»ÆĢ¼£» | |
| ¢Ü·“Ó¦½įŹųŹ±£¬ĻČ½«µ¼¹Ü“Ó×°ÖĆBÖŠ³·³ö£¬ŌŁĶ£Ö¹¼ÓČČ | ÄæµÄŹĒ·ĄÖ¹ŅŗĢåµ¹Į÷ŅżĘšŹŌ¹ÜÕØĮŃ£» | |
| ¢Ż“żŹŌ¹ÜĄäČ“ŗó½«Ź£Óą¹ĢĢåMµ¹ČėÉÕ±£¬¼ÓČė×ćĮæĻ”ĮņĖį£¬¹żĀĖ | µĆµ½Ą¶É«ĀĖŅŗ ĀĖŌüĪŖŗģÉ«ŗĶŗŚÉ«¹ĢĢå»ģŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
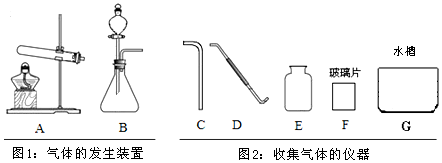
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
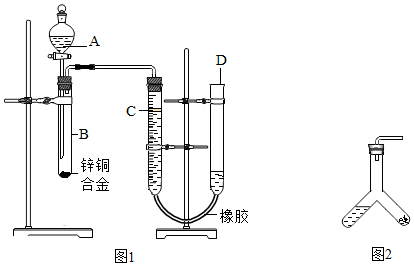
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×ÓÖŠŌ×ÓŗĖÄŚµÄÖŹ×ÓŹżŗĶÖŠ×ÓŹżŅ»¶ØĻąµČ | |
| B£® | Ķ¬ÖÖŌŖĖŲµÄŌ×ÓŗĶĄė×Ó£ØČēÄĘŌ×ÓŗĶÄĘĄė×Ó£©ŗĖÄŚÖŹ×ÓŹżŅ»¶ØĻąµČ | |
| C£® | ²Ī¼Ó»Æѧ·“Ó¦µÄø÷ĪļÖŹµÄ·Ö×Ó×ÜŗĶÓė·“Ó¦ŗóÉś³ÉµÄø÷ĪļÖŹµÄ·Ö×Ó×ÜŗĶĻąµČ | |
| D£® | »Æѧ·“Ó¦Ē°ŗó£¬Ō×ÓµÄÖÖĄą”¢ŹżÄæ”¢ÖŹĮ涼²»±ä |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com