
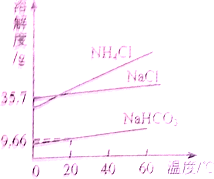
 实验室模拟“侯氏制碱法”制纯碱,其原理是NaCl+NH4HCO3=NaHCO3+NH4Cl,再将碳酸氢钠加热分解得到纯碱.如图是NaCl、NH4Cl、NaHCO3的溶解度曲线,下列说法正确的是( )
实验室模拟“侯氏制碱法”制纯碱,其原理是NaCl+NH4HCO3=NaHCO3+NH4Cl,再将碳酸氢钠加热分解得到纯碱.如图是NaCl、NH4Cl、NaHCO3的溶解度曲线,下列说法正确的是( )| A、NaHCO3从溶液中分离出,可采用的操作是蒸发结晶 | B、NH4Cl饱和溶液的溶质质量分数一定大于NaCl饱和溶液的溶质质量分数 | C、40℃时,溶解度大小关系是:NH4Cl>NaCl>NaHCO3 | D、20℃时,100g水中加入11.7g NaCl和15.8g NH4HCO3固体,充分反应后,理论上可析出7.14g NaHCO3晶体 |
 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:初中化学 来源: 题型:
| A、图书和精密仪器着火用干粉灭火器灭火 | B、炒菜时油锅着火,立即盖上锅盖 | C、用肥皂水检验液化气罐是否漏气 | D、天然气泄漏时,立即开窗通风 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 海洋中蕴含丰富的资源.
海洋中蕴含丰富的资源.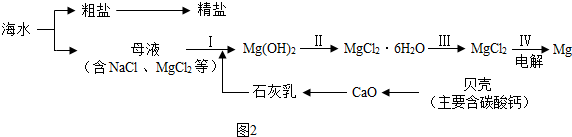
查看答案和解析>>
科目:初中化学 来源: 题型:
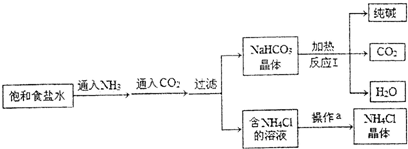
| A、使CO2更易被吸收 | B、NH3比CO2更易制取 | C、CO2的密度比NH3大 | D、为了增大NaHCO3的溶解度 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com