
| A. | D>A>B>C | B. | A>C>B>D | C. | C>D>A>B | D. | B>D>C>A |
科目:初中化学 来源: 题型:选择题

| A. | 20℃时,甲、乙的溶解度都是30克 | |
| B. | 40℃时,甲的溶解度小于乙的溶解度 | |
| C. | 升高温度能使乙的不饱和溶液变为饱和溶液 | |
| D. | 40℃时,甲的饱和溶液中溶质质量分数为50% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 表示一种原子,
表示一种原子, 表示另一种原子),从图中获得的有关信息不正确的是( )
表示另一种原子),从图中获得的有关信息不正确的是( )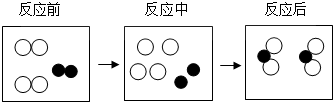
| A. | 化学反应中原子可以再分 | |
| B. | 化学反应中分子可以分为原子 | |
| C. | 化学反应中元素种类、原子种类和数目都没有改变 | |
| D. | 分子间存在一定的间隙 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 次数 | 加入稀硫酸的质量(g) | 反应后剩余的固体的质量(g) |
| 1 | 20 | 8.7 |
| 2 | 20 | m |
| 3 | 20 | 6.1 |
| 4 | 20 | 6.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
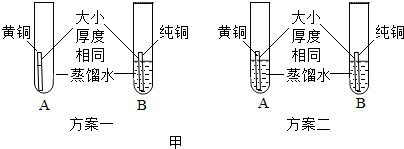

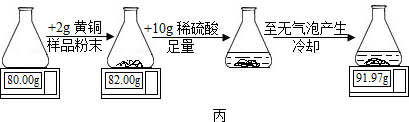
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com