
����Ŀ���α����ֽ���������������ķ�Ӧ�ж������̵Ĵ��������Լ���Ѱ���µĴ������о���ʵ�飬�����˻�ѧ̽��С�����Ȥ��
��������⣩�������ܷ�������������Һ�ֽ�Ĵ���������ܣ����Ч�����?
��ʵ��̽����
ʵ�鲽�� | ʵ������ |
�����ֱ���ȡ5mL5%����������Һ����A��B ��֧�Թ��У���A�Թ��м���ag��������ĩ�����ֱ���A��B��֧�Թ��в��������ľ�����۲����� | A�Թ��в������ݣ�������ľ����ȼ��B�Թ������������� |
������A�Թ���û��������ʱ�����¼������������Һ�����Ѵ����ǵ�ľ�������Թܣ���˷���������飬�۲����� | �Թ��о��������ݣ�������ľ������ȼ |
������ʵ�����е�ʣ����С�Ĺ��ˣ�����������������ϴ�ӡ�������������ù���������Ϊag�� | |
�����ֱ���ȡ5mL5%����������Һ����C��D ��֧�Թ��У���C�Թ��м���ag��������ĩ����D�Թ��м���ag�������̷�ĩ���۲����� |
��ʵ����ۣ�
��1��A�����������_____________��
��2��ʵ��������֤������������___________��____________�ڷ�Ӧǰ���û�з����仯������������������Һ�ֽ�Ĵ�����
��3��д��������������������Һ�ֽ�ķ��ű���ʽ__________________________��
��ʵ�����ۣ�
(1)ʵ���������Ŀ����__________________________________________��
(2)��ʵ�����۲쵽D�Թ��в������ݵ����ʸ��죬�ɴ�����Եõ��Ľ�����_______��
��ʵ����չ��
��1���������ϵ�֪��CuO��CuSO4����������Ҳ����������������Һ�ֽ�Ĵ����������йش�����˵������ȷ����______________������ţ���
A��MnO2ֻ��������������Һ�ֽ�Ĵ���
B��ͬһ����ѧ��Ӧ�����ж��ִ���
C������ֻ�ܼӿ컯ѧ��Ӧ������
D���������������ʲ�������������Ӧ�ķ�Ӧ���������
��2��ʵ�鴴������ѧ����Ϊ��Ҫ�Ŀ�ѧ��������ͼ��ijѧУ��ʦ������MnO2��H2O2��Һ�ֽ�ʵ��װ�õĴ����������ʵ��������£�
����һ֧���θ����ˮƽ���ã��õι���ȡ3ml(�ܶ�Ϊ1g/ml)��������Ϊ5%��H2O2�������ܵ������ڣ�����ҩ��ȡ0��2gMnO2��ĩ�����ڸ���ܵĽ����ܵĹܱ��ϡ�
����ȼ�����ϰ������������ܲ������������۲쵽�����ǵİ���������ȼ��
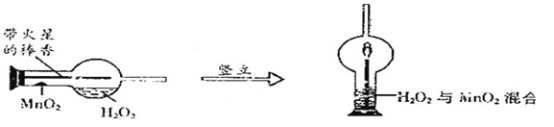
�Ըô���ʵ������ۣ�����Ϊ����������_________������ţ���
A��ʵ�������õ����������ϼ�ҩƷ���õ�
B��ʵ��ʹ�õ�ҩƷ����̫��
C����Ӧ�ٶ�̫��������ʱ��
D��ʵ���������ԣ�����װ�ú��Ƶ�ȼ�ĵ�����Ȥζ��ǿ
���𰸡�O2�� ���� ��ѧ���� 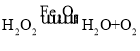 �Ƚ���������������̵Ĵ�Ч�� �������̵Ĵ�Ч������������ B B��C
�Ƚ���������������̵Ĵ�Ч�� �������̵Ĵ�Ч������������ B B��C
��������
��1��A�в�����������ʹ������ľ����ȼ��˵����������
��2���ж�һ�������Ƿ���ij��Ӧ�Ĵ�����Ҫ�����Ƿ�߱�����������������һ������������ܷ�ı䷴Ӧ�����ʣ���Ӧǰ�������������Ƿ�ı䣻�����Ļ�ѧ�����Ƿ�ı䡣ͨ����������֪�������������ͻ�ѧ�����ڷ�Ӧǰ���û�з����仯������������������Һ�ֽ�Ĵ�����
(3��������������������Һ�ֽ�ķ��ű���ʽΪ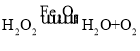 ��
��
[ʵ������]��֧�Թܶ�����ȡ5mL5%����������Һ��������Ĵ�����ͬ�������DZȽ���������������̵Ĵ�Ч����ʵ�����۲쵽D�Թ��в������ݵ����ʸ��죬˵���������̵Ĵ�Ч�����������á�
[ʵ����չ]��1��ֻ�о߱���һ��������� �������������͵ĸ÷�Ӧ�Ĵ�����������һ����ָ���Ǹı����ʷ�Ӧ�����ʣ����ı��������ӿ�ͼ����������棻����������������Ӧ�ķ�Ӧ����������������̣�ͬһ����ѧ��Ӧ�����ж��ִ������ʵ�飬���ܶ����ʲ����ض��Ĵ�������������̿����Ǵ���Ҳ�����Ǹ�����طֽ�������
��2��ֻ��Ҫ3ml(�ܶ�Ϊ1g/ml)��������Ϊ5%��H2O2 ��ҩƷ�������٣�B����ȼ�����ϰ������������ܲ������������۲쵽�����ǵİ���������ȼ��˵����Ӧ�ٶȺܿ죬C����ѡBC��


 ����ͬ�����Ծ�ϵ�д�
����ͬ�����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȤС��ͬѧ�Ӻ�ˮɹ�κ����±��ģ�ҵ��������ȡþ����Ҫ�������£�
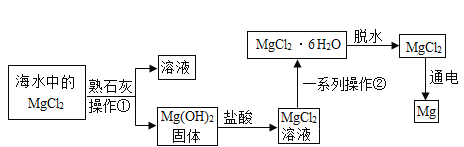
���������ۣ�
��1�������еIJ�������_______����ʵ��������ƣ���
��2��һϵ�в������а�������Ũ�� ��______�����˵ȡ�
��3������Ȼ�þ���Եõ�þ���������÷�Ӧ�Ļ�ѧ����ʽΪ��________���ñ仯������_______��ת��Ϊ��ѧ�ܡ�
��4��þ�Ļ�ѧ���ʱȽϻ��ã����ڵ�����ȼ�����ɵ���þ���ڵ���þ�е�Ԫ�صĻ��ϼ�Ϊ-3����þ�Ļ�ѧʽΪ��_______��
���������⣩þ��һ������ɫ�н�������Ľ��������ó���þ��������һ��Һ�ɫ��������"�����Һ�ɫ��������ʲô������?
���������ϣ���1��Mg(OH)2����ɫ���壬������ˮ�����Ȼ�ֽ������þ��ˮ��
��2��MgCO3�� ��ɫ���壬����ˮ�����Ȼ�ֽ������þ�Ͷ�����̼��
��3��MgCO3�����ȶ��Ա�Mg(OH)2�����ȶ��Ը�ǿ��
��������룩
С��ͬѧ��Ϊ�ù��岻������MgO��Mg(OH)2��MgCO3�����ǵ�������______��С��ͬѧ��ͭ��������Cu2(OH)2CO3���뵽�Һ�ɫ�����ʿ�����Mg2(OH)2CO3��
��ʵ�������
��ͼ��ʾװ�ý���ʵ�飬�����Թܿ���Һ�γ��֣�˵����Ӧ������______������ʯ��ˮ����ǣ�����ǵĻ�ѧ����ʽΪ__________����ͬʱ�Һ�ɫ������ȫ��Ϊ��ɫ�����Һ�ɫ������Mg2(OH)2CO3����д��Mg2(OH)2CO3���ȷֽ�Ļ�ѧ����ʽ__________��
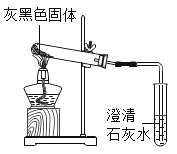
����ɲⶨ��
��ҵ�����еõ��ļ�ʽ̼��þ������xMgCO3yMg(OH)2zH2O��Ϊ��ȷ�����������ɣ�С��ͬѧȡ4.66g�þ��壬���ȷ����ǶԹ�������ȷֽ⣨����ʹ֮�ֽ⣬����ʧȥ�ᾧˮ�������ȫ��Ӧ�����ⶨʣ�����������ֽ��¶�֮���ϵ��
�����ݴ�����ʣ��������������ʱ���ϵ��ͼ��ʾ��
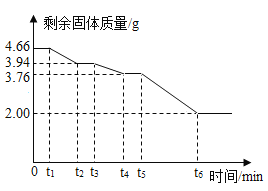
��ش��������⣺
��1��0��t1��������û�з����仯��ԭ�����______��
��2�������нᾧˮ������Ϊ_________g��
��3��t4��t5�ι���Ϊ______��MgO��д��ѧʽ����
��4������ͼ����������xMgCO3yMg(OH)2zH2O��x��y��z������= ______����д��Ҫ���̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ѧϰ�˶������̶Թ�������ֽ��д����õ�֪ʶ�������˻�ѧ̽��С�����Ȥ��
��������⣩
����ͭ�ܷ�������������Һ�ֽ�Ĵ�����
��ʵ��̽����
ʵ�鲽�� | ʵ������ |
�ֱ���ȡ5mL 5%����������Һ����A��B��֧�Թ��У���A�Թ��м���ag����ͭ��ĩ�����ֱ���A��B��֧�Թ��в��������ľ�����۲����� | A�Թ��в������ݣ�������ľ�� ��ȼ��B�Թ������������� |
��A�Թ���û��������ʱ�����¼������������Һ�����Ѵ����ǵ�ľ�������Թܣ���˷���������飬�۲����� | �Թ��о��������ݣ�������ľ ������ȼ�� |
��ʵ��II�е�ʣ����С�Ĺ��ˣ�����������������ϴ�ӡ�������������ù���������Ϊag�� |
��ʵ����ۣ�
��1����ʵ�������Եó��Ľ�����__________�ܼӿ��������ֽ��������������ʡ�
��2��ʵ���֤��������ͭ��___________��__________�ڷ�Ӧǰ���û�з����仯����������������ֽ�Ĵ�����
��3����������������ͭ�Ĵ��·ֽ�ų�������Ӧ�����ֱ���ʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������û�ѧѧ����ʶ����ķ�ʽȫ���˽���ʶ����������
��1�������ʷ���Ƕȣ����ʵĿ�������________(�����������������������)
��2���ӹ������ʵ����Ƕ���������ʾ��ԭ��,������ʾ��ԭ��
������![]() ���ɱ�ʾ������________
���ɱ�ʾ������________
��ͬ�¶��£����������ȵ��ڷ�����Ŀ�ȡ��������������ɷֺ��Բ��ƣ����пɱ�ʾ������ģ�͵���__________(�����)
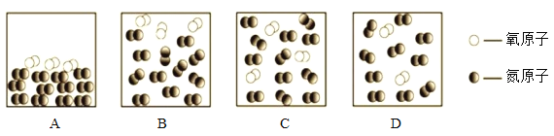
��3���ӻ����Ƕ�:�������������ھ�����������_________(�����)
��ʹ�������Դ����ú��ʯ�� �ڶ�ʹ��������������
��ʵʩ�̻����̣������ﳾ��Ⱦ �ܷ��������������¶�����
��4����ͼΪһ�����ͻ�����,��ͨ�� 360����ת��������Ͳ����������ˮ���Ӷ����⼫�˶����������˴����IJ��ʡ�������������ˮ��������________

��5��ʵ��̽���Ƕ�:��ͼ��ʾ��ʵ����п����ɷֵIJⶨ��
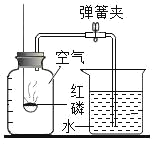
��ʵ��ǰ,Ӧ���ȼ��__________ȷ��ʵ��ɹ���
��д������ȼ�յĻ�ѧ����ʽ________��ʵ���к���Ӧȡ������ԭ��________
��ʵ����,������ƿ��ȴ������ʱ,���ɼ�,�۲쵽��������________
�ܸ�ʵ�����ܲ�����ľ̿�������,��˵������________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ֱ�ӽ���ˮ����Ϊ����ˮ����Ҫ��������������ˮ�ľ����������ƣ���ͼ��ʾ�����������ӽ�����֬����Ҫ������ȥ���ؽ������ӡ�����ˮ�ʣ�
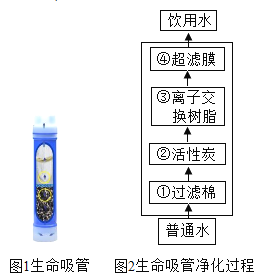
��1�����л���̿��������_________������ĸ����ͬ�������г���Ĥ��������_________��
A ȥ���к����Ͳ��ֲ���
B ����ɫ�غ���ζ
C ��ȥ�ϴ�IJ���������
��2��ȡ�ú�ˮʱ��Ҫ����ˮ��Ӳ�Ⱥ�ɱ��ԭ��������г���ȡ����_________��
��3������ˮ�����У�ˮ�տ�ʱ�������������DZ������ˣ��Դ��۵ĽǶȽ�����һ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ij��ѧ��Ӧ�и�����������ʱ��ı仯��ϵ��������������ȷ���ǣ� ��
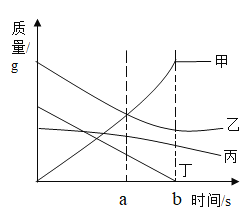
A. aʱ��ʱ�������ʵ�������ϵһ���Ǽ�=��+��+��
B. �÷�Ӧ��bʱ��ʱ����
C. ��Է���������>��>��>��
D. �÷�Ӧ�����Ļ�����Ӧ����Ϊ�ֽⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�ط��š���ѧʽ�����ӷ��ŵȻ�ѧ�����ʾ��
��1����Ԫ��___
��2��2����ԭ��________
��3��2H��_____
��4��3��������̼����______
��5������þ����_____
��6����ԭ�ӵĽṹʾ��ͼ___________
��7�������ӵĽṹʾ��ͼ_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ���ѧϰ���о���ѧ����Ҫ���ߡ�������±���Ԫ�����ڱ��IJ������ݣ��ش��й����⡣

��1������ϱ��в������̼Ԫ�ص�һ����Ϣ____________��
��2����3���ڣ����У������ڽ���Ԫ�ص���________����һ�֣�������������________�������ӷ��ţ�
��3����11��Ԫ�����17��Ԫ����ɵ�������________ �����ɸ����ʵ�����___________����������������ԭ������������������
��4����Ԫ�����ڱ��У�ͬһ�壨���У���Ԫ�ؾ������ƵĻ�ѧ���ʡ������и���Ԫ�ؾ������ƻ�ѧ���ʵ���__________________�����ţ���
a��He��Ne b��B��Mg c��Al��Si d��F��Cl
��5����2��3���ڵ�Ԫ�أ�������______�������������� ���ǽ�������Ԫ�ؿ�ͷ����__________Ԫ�ؽ�β��
��6��д��һ����������Ԫ��ԭ�ӵĺ�������Ų�����______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˷������������ĺ�����ijѧϰС�������ʵ���о�����ȡ6g������10%�����ᷴӦ���������˼�������������ų����������Ĺ�ϵͼ����ͼ����
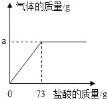
˵�������������ʲ�����ˮ���������ᷴӦ��
��1������ȫ��Ӧ��ȥ���������Ϊ_____g��
��2��������������������Ϊ���٣���д��������̣����������С�����һλ��_____��
��3��ijͬѧ�г������¼���ʽ������������պ÷�Ӧ��ȫʱ������Һ��������73+6��a��gС���Ըü���ʽ��������ɣ���ָ�����еĴ���_____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com