
| A. | 把实验剩余的药品倒入废液缸 | |
| B. | 用药匙取用食用盐,再用同一药匙直接取用碳酸钠粉末 | |
| C. | 取用较多量液体药品时,可直接向试管中倾倒 | |
| D. | 向试管中倾倒液体时,试管要直立 |
分析 A、做实验时剩余药品不能随意丢弃,要放入教师指定容器中,据此分析判断;
B、根据药匙使用的注意事项分析判断;
C、根据液体药品取用的方法分析判断;
D、根据液体药品取用的方法分析判断.
解答 解:A、做实验时剩余的药品不能随意丢弃,不能带出实验室、不能放回原瓶,要放到教师指定的容器中,故A不正确;
B、用药匙取用药品后要用洁净的纸将药匙擦干再去取用另一种药品,以免污染药品,故B不正确;
C、取用较多量液体药品时,可用试剂瓶向试管中直接倾倒,故C正确;
D、向试管中倾倒液体药品时,试管要倾斜,故D不正确;
故答案为C.
点评 此题考查常见的固体药品取用和液体药品取用,属于基础考查,掌握相应的操作方法,养成良好的操作习惯是顺利进行实验和进一步学好化学的基础.


科目:初中化学 来源: 题型:选择题
| A. | 大于8mL | B. | 小于8mL | C. | 等于8mL | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物 质 | 杂 质 | 试 剂 | 操 作 | |
| A | Fe | Fe2O3 | 盐酸 | 结晶 |
| B | NH4HCO3 | NaCl | - | 加热 |
| C | Cu(NO3)2溶液 | BaCl2 | AgNO3溶液 | 过滤 |
| D | O2 | 水蒸气 | 浓硫酸 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 化学兴趣小组的同学们用下列药品探究影响金属与酸反应速率的因素.装置中产生氢气的量可以用压强传感器测出(在等温条件下,产生氢气体积与装置内压强成正比.反应放热忽略不计)
化学兴趣小组的同学们用下列药品探究影响金属与酸反应速率的因素.装置中产生氢气的量可以用压强传感器测出(在等温条件下,产生氢气体积与装置内压强成正比.反应放热忽略不计)查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 方案编号 | 方案1 | 方案2 |
| 实验操作 (分别取少量实验后的溶液于试管中) | 加入少许氧化铁 | 滴加硝酸银溶液 |
| 实验现象 | 固体逐渐消失,溶液由无色变成黄色 | 产生白色沉淀. |
| 实验结论 | 猜想二成立. | |
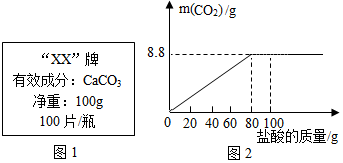
| 第1次 | 第3次 | 第4次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | a | 20 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验结果 |
| (1)取少量试剂瓶内溶液于试管中,并加入过量酚酞试液. | 溶液呈红色 |
| (2)再向上述溶液中加入适量BaCl2溶液. | 有白色沉淀生成 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 测定空气中氧气的含量时,实验结果小于$\frac{1}{5}$--红磷过量 | |
| B. | 经过多次过滤的河水仍然浑浊--滤纸破损 | |
| C. | 点燃氢气时突然发生爆炸--点燃前没有检验纯度 | |
| D. | 制取CO2时始终没有收集到CO2--装置气密性不好 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com