
·ÖĪö øł¾ŻŅŃÓŠµÄĪļÖŹµÄŠŌÖŹ½ųŠŠ·ÖĪö£¬£Ø1£©¼×”¢ŅŅ”¢±ū¾łĪŖŃõ»ÆĪļ£¬ŌŚ³£ĪĀĻĀŅĄ“ĪĪŖĘų”¢Ņŗ”¢¹ĢĢ¬£¬¼×-ŅŅ-±ū£¬ŌņŅŅĪŖĖ®£¬¼×ĪŖ¶žŃõ»ÆĢ¼£¬±ūĪŖŃõ»ÆøĘ£¬£Ø2£©ŅŅŗĶ±ū·¢ÉśµÄŹĒÖŠŗĶ·“Ó¦£¬ŌņŅŅŗĶ±ūĪŖĖįŗĶ¼īµÄ·“Ó¦£¬¼×ÓÉČżÖÖŌŖĖŲ×é³É£¬Ōņ¼×æÉÄÜĪŖĢ¼ĖįøĘ£¬ŅŅæÉÄÜĪŖŃĪĖį£¬±ūæÉÄÜĪŖĒāŃõ»ÆøĘ£¬Č»ŗó½«ĶĘ³öµÄĪļÖŹ½ųŠŠŃéÖ¤¼“æÉ£®
½ā“š ½ā£ŗ£Ø1£©¼×”¢ŅŅ”¢±ū¾łĪŖŃõ»ÆĪļ£¬ŌŚ³£ĪĀĻĀŅĄ“ĪĪŖĘų”¢Ņŗ”¢¹ĢĢ¬£¬¼×-ŅŅ-±ū£¬ŌņŅŅĪŖĖ®£¬¼×ĪŖ¶žŃõ»ÆĢ¼£¬±ūĪŖŃõ»ÆøĘ£¬ĖłŅŌ±ūµÄĖ׳ĘĪŖÉśŹÆ»Ņ£¬¼×ÓėŅŅµÄ·“Ó¦Ź±¶žŃõ»ÆĢ¼ŗĶĖ®·“Ӧɜ³ÉĢ¼Ėį£¬»Æѧ·½³ĢŹ½ĪŖ£ŗH2O+CO2ØTH2CO3£»
£Ø2£©ŅŅŗĶ±ū·¢ÉśµÄŹĒÖŠŗĶ·“Ó¦£¬ŌņŅŅŗĶ±ūĪŖĖįŗĶ¼īµÄ·“Ó¦£¬¼×ÓÉČżÖÖŌŖĖŲ×é³É£¬Ōņ¼×æÉÄÜĪŖĢ¼ĖįøĘ£¬ŅŅæÉÄÜĪŖŃĪĖį£¬±ūæÉÄÜĪŖĒāŃõ»ÆøĘ£¬ĖłŅŌ¼×µÄ»ÆѧŹ½ĪŖ£ŗCaCO3£¬ŅŅÓė±ūµÄ·“Ó¦Ź±ŃĪĖįŗĶĒāŃõ»ÆøĘ·“Ӧɜ³ÉĀČ»ÆøĘŗĶĖ®£¬»Æѧ·½³ĢŹ½ĪŖ£ŗ2HCl+Ca£ØOH£©2 ØTCaCl2+2H2O£®
¹Ź“š°øĪŖ£ŗ£Ø1£©ÉśŹÆ»Ņ£¬CO2+H2OØTH2CO3£»
£Ø2£©CaCO3£¬2HCl+Ca£ØOH£©2 ØTCaCl2+2H2O£®
µćĘĄ ŌŚ½ā“ĖĄąĢāŹ±£¬Ź×ĻČ½«ĢāÖŠÓŠĢŲÕ÷µÄĪļÖŹĶĘ³ö£¬Č»ŗó½įŗĻĶĘ³öµÄĪļÖŹŗĶĢāÖŠµÄ×Ŗ»Æ¹ŲĻµĶʵ¼Ź£ÓąµÄĪļÖŹ£¬×īŗó½«ĶĘ³öµÄø÷ÖÖĪļÖŹ“śČė×Ŗ»Æ¹ŲĻµÖŠ½ųŠŠŃéÖ¤¼“æÉ£®


 ÓŵČÉśĢāæāĻµĮŠ“š°ø
ÓŵČÉśĢāæāĻµĮŠ“š°ø 53ĢģĢģĮ·ĻµĮŠ“š°ø
53ĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ĪĀ¶Č/”ę | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| Čܽā¶Č/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
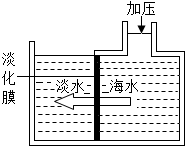 µ»Æŗ£Ė®æɲÉÓĆĤ·ÖĄė¼¼Źõ£ØČēĶ¼£©£¬Ė®·Ö×ÓæÉŅŌĶø¹żÄ¤£Øŗ£Ė®ÖŠĘäĖūĮ£×Ó²»ÄÜĶø¹ż£©½ųČė×ó²ąµÄ³Ų×Ó£¬“Ó¶ųµĆµ½µĖ®£®ŅŌĻĀ·ÖĪöÖŠÕżČ·µÄŹĒ£Ø””””£©
µ»Æŗ£Ė®æɲÉÓĆĤ·ÖĄė¼¼Źõ£ØČēĶ¼£©£¬Ė®·Ö×ÓæÉŅŌĶø¹żÄ¤£Øŗ£Ė®ÖŠĘäĖūĮ£×Ó²»ÄÜĶø¹ż£©½ųČė×ó²ąµÄ³Ų×Ó£¬“Ó¶ųµĆµ½µĖ®£®ŅŌĻĀ·ÖĪöÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | ÕāÖÖĤæÉÓĆĀĖÖ½“śĢę | B£® | ×ó²ą³ŲÖŠµÄµĖ®ŹōÓŚ»ģŗĻĪļ | ||
| C£® | ÓŅ²ą³ŲÖŠČܼĮµÄÖŹĮæ¼õÉŁ | D£® | ÓŅ²ą³ŲÖŠŗ£Ė®µÄČÜÖŹÖŹĮæ·ÖŹż²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “æŃņĆ«ÉĄ-ĢģČ»ĻĖĪ¬ | B£® | ²»ŠāøÖ²Ķ¾ß-ĢśŗĻ½š | ||
| C£® | ןŹÆ-½šøÕŹÆ | D£® | Ęū³µĀÖĢ„-ĖÜĮĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
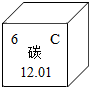 Ģ¼¼Ņ×åŹĒ»ÆѧŹĄ½ēÖŠ×īÅÓ“óµÄ¼Ņ×壬Ģ¼¼°Ęä»ÆŗĻĪļŌŚÉś²śÉś»ī֊ӊ׏ć·ŗÓ¦ÓĆ£®
Ģ¼¼Ņ×åŹĒ»ÆѧŹĄ½ēÖŠ×īÅÓ“óµÄ¼Ņ×壬Ģ¼¼°Ęä»ÆŗĻĪļŌŚÉś²śÉś»ī֊ӊ׏ć·ŗÓ¦ÓĆ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
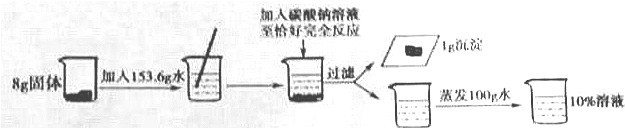
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H+”¢Cl-”¢HCO3- | B£® | Ca2+”¢CO32-”¢NO3- | C£® | NH4+”¢OH-”¢NO3- | D£® | Na+”¢Fe2+”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com