
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样品少量于小烧杯中,加入适量水,充分搅拌,过滤. | ||
| ②______. | 大量气泡 产生 | 氢氧化钙已经变质. |
| ③取少量滤液于试管中,______. | ______ | 氢氧化钙没有完全变质. 该反应的化学方程式为______. |
| 实验步骤 | 实验现象 | 实验结论 |
| ②取少量滤渣与试管中,滴加适量稀盐酸 | ||
| ③通入二氧化碳 | 有白色沉淀产生 | CO2+Ca(OH)2=CaCO3↓+H2O |
| 实验步骤 | 实验现象 | 实验结论 |
| ②滴加适量稀盐酸 | ||
| ③通入二氧化碳 | 有白色沉淀产生 | CO2+Ca(OH)2=CaCO3↓+H2O |


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:初中化学 来源: 题型:阅读理解
| 小资料:无水硫酸铜为 白色粉末,遇水变蓝. |
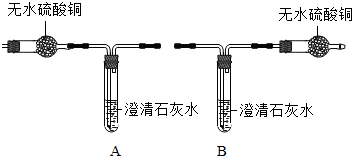
| 实验操作与现象 | 实验结论 |
取少量黑色粉末于试管中,加入足量的稀硫酸,加热,观察到黑色粉末全部溶解,溶液变为蓝色 取少量黑色粉末于试管中,加入足量的稀硫酸,加热,观察到黑色粉末全部溶解,溶液变为蓝色 |
猜想②正确 |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
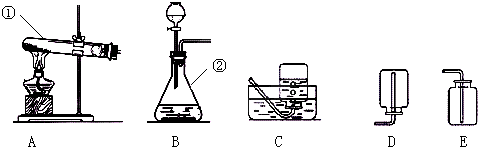
| ||
| ||
| ||
| ||
| 实验操作步骤 | 实验现象 | 实验结论 |
| ①取样品于试管中,加入适量水,充分振荡后静置并滴加几滴无色酚酞 ②或取样品于试管中,加入适量的稀盐酸 |
①试管中的液体呈红色 ② 没有气泡冒出 没有气泡冒出 |
①样品中含有: 氢氧化钙 氢氧化钙 ②样品中不含有碳酸钙. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验操作 | 实验现象 | 解释和结论 | |||||||||
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 产生的气泡很少,木条不复燃 | 常温下H2O2溶液分解速率非常缓慢,放出极少量的氧气,因此木条不复燃. | ||||||||
| 实验二 | 向盛水的试管中加入氧化铁,伸入带火星的木条 | 没有明显现象 | 氧化铁加入水中不产生氧气 氧化铁加入水中不产生氧气 | ||||||||
| 实验三 | 取5mL5%的过氧化氢溶液于试管中,再加入一定量的氧化铁,伸入带火星的木条 | 有大量气泡产生 有大量气泡产生 带火星的木条复燃 带火星的木条复燃 |
氧化铁能加快过氧化氢的分解.反应的化学方程式是 2H2O2
2H2O2
|
| 实验目的 | 实验操作及现象 | 实验结论 | |
| 补充实验一 | 探究在反应前后固体的质量是否改变 探究在反应前后固体的质量是否改变 |
从上述实验三中回收剩余固体,洗涤、干燥后称量,比较固体在过氧化氢分解前后的质量. 从上述实验三中回收剩余固体,洗涤、干燥后称量,比较固体在过氧化氢分解前后的质量. |
在反应前后固体的质量没变. |
| 补充实验二 | 探究在反应前后固体的化学性质是否改变 | 从上述实验三中回收剩余固体,洗涤后再加入过氧化氢溶液,仍有能使带火星木条复燃的气体产生. | 在反应前后固体的化学性质没变 在反应前后固体的化学性质没变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 小资料:无水硫酸铜为 白色粉末,遇水变蓝. |
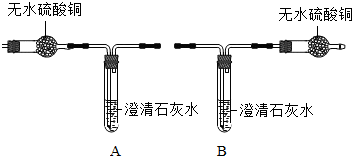
| 实验操作与现象 | 实验结论 |
| ________ | 猜想②正确 |
查看答案和解析>>
科目:初中化学 来源:2012-2013学年北京市大兴区九年级(上)期末化学试卷(解析版) 题型:解答题
| 小资料:无水硫酸铜为 白色粉末,遇水变蓝. |
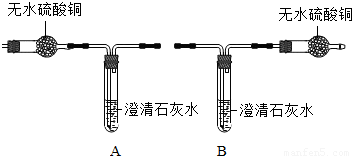
| 实验操作与现象 | 实验结论 |
| ______ | 猜想②正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com