
分析 根据物质的结构决定物质的性质,物质的性质决定物质的用途解答.
解答 解:(1)制肥皂,其水溶液能使酚酞溶液变红的是氢氧化钠.故填:②;
(2)硝酸钾中含有氮元素和钾元素两种营养元素,属于复合肥.故填:④;
(3)聚乙烯属于合成材料,故填:③;
(4)熟石灰显碱性,能和酸性物质反应.故填:①;
(5)钛合金密度小,可用来制造人造骨,故填:⑦;
(6)氮气化学性质稳定,焊接金属时常用作保护气,故填:⑤;
(7)生石灰具有吸水性,常用作干燥剂,故填:⑥.
答案:(1)②;(2)④;(3)③;(4)①;(5)⑦;(6)⑤;(7)⑥.
点评 物质的性质决定用途,同学们要熟悉常见物质的性质,并能根据物质的性质推测物质的用途.


科目:初中化学 来源: 题型:选择题
| A. | 麻黄碱的相对分子质量为165 | |
| B. | 麻黄碱中含有10个碳原子 | |
| C. | 麻黄碱中氢元素的质量分数最大 | |
| D. | 麻黄碱中氮元素和氧元素的质量比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是硝酸钾和碳酸钾在不同温度时的溶解度曲线和溶解度数据表.
如图是硝酸钾和碳酸钾在不同温度时的溶解度曲线和溶解度数据表.| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |
| K2CO3 | 110 | 114 | 121 | 126 | 139 | |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
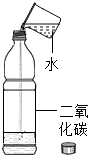 如图,向一个集满二氧化碳的质地较软的塑料瓶中加入约$\frac{1}{2}$体积的水,立即旋紧瓶盖,振荡,可以看到塑料瓶变瘪,此实验说明二氧化碳能溶于水,此实验说明不能(“能”、“不能”)说明二氧化碳与水反应生成碳酸.
如图,向一个集满二氧化碳的质地较软的塑料瓶中加入约$\frac{1}{2}$体积的水,立即旋紧瓶盖,振荡,可以看到塑料瓶变瘪,此实验说明二氧化碳能溶于水,此实验说明不能(“能”、“不能”)说明二氧化碳与水反应生成碳酸.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 物质之间发生化学反应时常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.
物质之间发生化学反应时常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某班同学为证明NaOH能与稀盐酸发生中和反应,从不同角度设计了如下实验方案,并进行实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com