
分析 (1)根据灭火的原理和燃烧的条件分析;
(2)根据反应的剧烈程度不同分析;
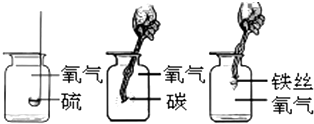
(3)硫、铁丝、木炭与氧气反应分别生成二氧化硫、四氧化三铁和二氧化碳,都属于化合反应,也属于氧化反应,并且都是在点燃的条件下才能燃烧,反应都放出热量等;而不同之处主要在于它们的生成物的状态,产生的火焰等方面;
(4)做铁丝在氧气中燃烧实验时,集气瓶底要放少量水或细沙,防止高温生成物溅落瓶底,使集气瓶底炸裂;硫燃烧生成的二氧化硫有毒能污染空气,能溶于水,故可用水吸收.
解答 解:(1)水可以吸收热量,降低可燃物的温度,所以硫燃烧实验即将结束时,可将燃烧匙底部接触水即可使火焰熄灭,其原理是降低可燃物的温度至着火点以下;刚点燃火柴就伸入氧气中火柴消耗的氧气太多致使看不到铁丝燃烧,故答案:降低可燃物的温度至着火点以下;为防止火柴燃烧消耗集气瓶中的氧气;
(2)硫是一种淡黄色固体,在空气中燃烧发出淡蓝色火焰,在氧气中燃烧发出明亮的蓝紫色火焰,产生一种具有刺激性气味的气体;在空气里和氧气里燃烧的现象不同,说明了可燃物燃烧时与氧气的浓度有关,浓度越大燃烧越剧烈;故答案为:淡蓝色;蓝紫色;可燃物燃烧时与氧气的浓度有关,浓度越大燃烧越剧烈.
(3)根据图中所发生的化学反应,进行总结归纳它们的共同点为:①反应物都有氧气;②反应条件为点燃;③都为化合反应;④都是氧化反应,⑤都放热等;根据它们反应后的生成物可以知道,硫燃烧产生了二氧化硫为气体,铁丝燃烧产生了四氧化三铁为固体,木炭燃烧产生了二氧化碳气体,故它们的产物的状态不同.故答案为:反应条件为点燃(或反应物都有氧气或都是氧化反应等);产物的状态不同(合理即可);
(4)做铁丝在氧气中燃烧实验时,集气瓶底要放少量水或细沙,防止高温生成物溅落瓶底,使集气瓶底炸裂.由于硫燃烧生成的二氧化硫有毒能污染空气,二氧化硫能溶于水,所以做硫燃烧的实验时集气瓶底放少量的水的目的是:吸收生成的二氧化硫防止污染空气.所以硫、铁丝燃烧实验中用到的氧气,最好采用排水法收集.
故答案为:防止高温生成物溅落瓶底,使集气瓶底炸裂;二氧化硫有毒能污染空气,二氧化硫能溶于水,细沙不能吸收二氧化硫;二氧化硫能溶于水;排水.
点评 熟练掌握氧气的化学性质,并熟记常见物质在氧气中燃烧的现象和产物,才能顺利解答.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:多选题
| A. | 催化剂能改变化学反应速率 | |
| B. | 反应后催化剂的化学性质会改变 | |
| C. | 反应后催化剂的质量不变 | |
| D. | 催化剂在实际生产和生活中没有实际意义 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
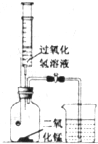 用如图装置,在常温下进行探究燃烧条件的实验.烧杯中盛有80℃热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞,推入适量过氧化氢溶液,打开止水夹.(白磷的着火点为40℃.)
用如图装置,在常温下进行探究燃烧条件的实验.烧杯中盛有80℃热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞,推入适量过氧化氢溶液,打开止水夹.(白磷的着火点为40℃.)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 我校化学兴趣小组同学为了测定石灰石中碳酸钙的质量分数,将15g石灰石样品加入到73g稀盐酸中恰好完全反应(杂质不溶于水,也不与盐酸反应),产生CO2气体的情况如图所示.计算:
我校化学兴趣小组同学为了测定石灰石中碳酸钙的质量分数,将15g石灰石样品加入到73g稀盐酸中恰好完全反应(杂质不溶于水,也不与盐酸反应),产生CO2气体的情况如图所示.计算:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碳酸钠溶液和氯化钙溶液 | B. | 氢氧化钾溶液与盐酸 | ||
| C. | 氢氧化钠溶液与氯化钾溶液 | D. | 硫酸铜溶液与氯化钡溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
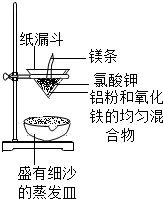 铝和氧化铁的反应:2A1+Fe2O3$\frac{\underline{\;900℃~1550℃\;}}{\;}$Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该溶融物可用于焊接铁轨.
铝和氧化铁的反应:2A1+Fe2O3$\frac{\underline{\;900℃~1550℃\;}}{\;}$Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该溶融物可用于焊接铁轨.| 物质 | A1 | Al2O3 | Fe | Fe203 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量冷却后的熔融物于试管中,加入氢氧化钠溶液 | 产生气泡 | 熔融物中含有铝 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 药品柜 | 甲 | 乙 | 丙 | 丁 |
| 药品 | 硫酸、硝酸 | 氢氧化钠、氢氧化钙 | 氯化钠、硫酸钾 | 汽油、酒精 |
| A. | 甲 | B. | 乙 | C. | 丙 | D. | 丁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com