
| A. | pH等于8的溶液一定是碱的溶液 | |
| B. | 不饱和溶液变为饱和溶液溶质质量分数一定变大 | |
| C. | 所有的酸与活泼金属反应一定能生成氢气 | |
| D. | 金属与酸溶液发生置换反应时,生成的溶液质量一定大于原来酸溶液的质量 |
分析 A、根据pH与溶液酸碱性的关系分析,pH等于8的溶液是碱性的溶液;
B、通过改变温度将不饱和溶液析出晶体后变为饱和溶液的情况,溶质质量分数变小;
C、根据酸跟活泼金属反应不一定生成氢气分析;
D、根据金属与酸溶液发生置换反应,金属成为离子进入溶液,氢被置换出来成为氢气逸出溶液分析.
解答 解:A、pH等于8的溶液是碱性的溶液,不一定是碱溶液,故说法错误;
B、通过改变温度将不饱和溶液析出晶体后变为饱和溶液的情况,溶质质量分数变小,故说法错误;
C、酸跟活泼金属反应不一定生成盐和氢气,例如稀硝酸和锌反应能生成硝酸锌、水和一氧化氮,不能生成氢气,故说法错误;
D、金属与酸溶液发生置换反应,金属成为离子进入溶液,氢被置换出来成为氢气逸出溶液,由于参加反应的金属的质量大于生成的氢气的质量,因此所得溶液质量一定大于原来酸溶液的质量,故说法正确;
故选D.
点评 本题难度较大,掌握pH与溶液酸碱性的关系、不饱和溶液变为饱和溶液的方法以及金属与酸反应的知识即可解答,注意:碳酸盐的检验方法.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
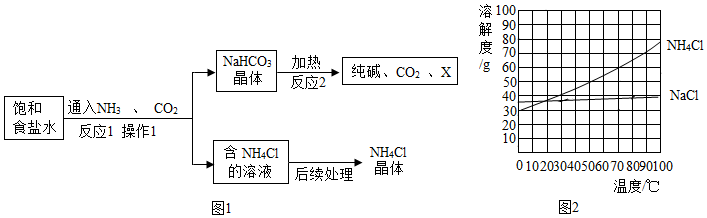
 “侯氏制碱法”的生产原理是:先将氨气通入饱和食盐水中,再将压缩的二氧化碳通入饱和的氨盐水,得到碳酸氢钠晶体,分离得到的碳酸氢钠晶体充分受热分解后即可制得纯碱.
“侯氏制碱法”的生产原理是:先将氨气通入饱和食盐水中,再将压缩的二氧化碳通入饱和的氨盐水,得到碳酸氢钠晶体,分离得到的碳酸氢钠晶体充分受热分解后即可制得纯碱.| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | |
| 溶解度 (g/100g水) | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 加入盐酸质量(g) | 20 | 40 | 60 | 80 | 100 | 120 |
| 收集的气体质量(g) | 0.88 | a | 2.64 | 3.52 | 4.4 | 4.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO+CuO$\stackrel{△}{→}$Cu+CO2↑ | B. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | ||
| C. | CaCO3→CaO+CO2↑ | D. | CO+O2 $\stackrel{点燃}{→}$ CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金刚烷中C、H原子的个数比为5:8 | |
| B. | 金刚烷的化学式为C10H16 | |
| C. | 金刚烷是一种无机物 | |
| D. | 金刚烷中氢元素的质量分数约为11.76% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com