

分析 (1)根据目前人们所使用的三大化石燃料煤、石油、天然气进行分析;
(2)①根据天然气和煤燃烧后的产物来分析;②根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;
根据化学方程式进行计算解答;
③根据化学方程式进行计算;
解答 解:(1)目前人们所使用的三大化石燃料是指煤、石油和天然气,故填:石油;
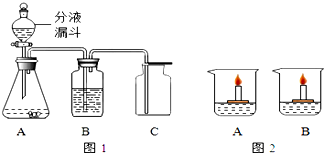
(2)①根据图示可知,天然气和煤燃烧后都会产生二氧化碳气体,等质量的天然气完全燃烧产生的二氧化硫比等质量的煤完全燃烧产生的二氧化硫少很多,因此燃煤更容易导致酸雨,对环境影响比较大;二者燃烧都会产生导致温室效应的二氧化碳气体;因为天然气燃烧后会产生二氧化硫,说明天然气中含有硫元素;故填:A;
②天然气的主要成分是甲烷,甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;设燃烧xg甲烷生成二氧化碳的质量为2500g,则:
CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
16 44
xg 2500g
$\frac{16}{44}=\frac{xg}{2500g}$
x≈909g
$\frac{909g}{1000g}×100%$=90.9%
故由计算可知,该天然气中甲烷的含量约为90.9%;
③由图示可知,燃烧1000g煤生成二氧化硫的质量为11g,设燃烧 1kg 煤至少需要约xg10%的氢氧化钠溶液治理废气.则:
2NaOH+SO2═Na2SO3+H2O
80 64
10%xg 11g
$\frac{80}{64}=\frac{10%xg}{11g}$
x=137.5g
故故由计算可知,燃烧 1kg 煤至少需要约137.5g10%的氢氧化钠溶液治理废气.
故答案为:(1)石油;(2)①A;②CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;90.9%;③137.5g;
点评 本题考查三大化石燃料,化学方程式的书写及有关化学方程式的计算等,基础性较强,要牢固掌握.


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
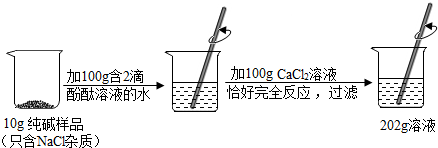
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
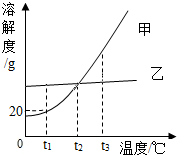 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )| A. | 甲的溶解度比乙的溶解度大 | |
| B. | t1℃时,100g甲饱和溶液中溶质的质量是20g | |
| C. | t2℃时,甲、乙的两种饱和溶液中溶质的质量分数相等 | |
| D. | 将等质量甲、乙的两种溶液分别由t1℃降至t2℃,析出甲的质量一定比析出乙的质量大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 ”和“
”和“ ”分别表示氮原子和氢原子,如图是氮气与氢气在高温催化剂条件下发生反应的微观模拟图.请根据此图回答下列问题:
”分别表示氮原子和氢原子,如图是氮气与氢气在高温催化剂条件下发生反应的微观模拟图.请根据此图回答下列问题: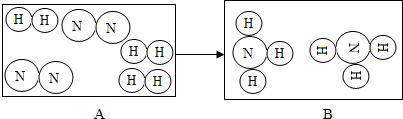
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 5.0 | 1.2 | 2.0 | 0.4 |
| 反应后质量(g) | 待测 | 3.0 | 3.6 | 0.4 |
| A. | 甲是反应物,乙、丙是生成物 | B. | 丁可能是催化剂 | ||
| C. | 反应后甲的质量是3.4g | D. | 甲一定是化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com