
| A. | 若是镁铝合金,则X<0.4g | |
| B. | 若是镁铝合金,则X>0.4g | |
| C. | 若是镁铜合金,则稀盐酸溶质的质量分数小于14.6% | |
| D. | 若是镁铁合金,X=0.32g,则合金中镁的质量分数是60% |
分析 因为金属与酸反应时生成氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}$×金属的质量,所以同质量镁与酸反应生成氢气的质量均大于铁、锌,而小于铝.据此分析解答即可.
解答 解:假设合金中镁的质量为4.8g,则根据化学反应的方程式:Mg+2HCl=MgCl2+H2↑可计算出此时产生氢气的质量为0.4g,同理可计算出4.8gAl与足量盐酸反应产生氢气的质量大于0.4g,4.8gZn与足量盐酸反应产生氢气的质量小于0.4g,4.8gFe与足量盐酸反应产生氢气的质量小于0.4g,
A、若混合物为Mg、Al,m一定大于0.4g,故A错误;
B、若混合物为Mg、Al,m一定大于0.4g,故B正确;
C、当粉末为Mg、Cu合金时,因铜不和盐酸反应,而4.8g镁时,消耗氯化氢的质量为14.6g,所以合金为为镁铜合金时,所需盐酸溶质质量分数一定小于14.6%,故C正确;
D、若混合物为Mg、Fe,X=0.32g,则合金中镁的质量分数是60%,故D正确.
故选:A.
点评 相同质量的金属与酸反应产生氢气的质量的多少与金属的相对原子质量有关.若相对原子质量越大,产生的氢气质量越小.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
 (1)活性炭是防毒面具滤毒罐里的吸附剂,可用来吸附氯气等有毒气体.如表列出了一定温度和压强下每立方厘米活性炭所能吸附的常见气体的体积.
(1)活性炭是防毒面具滤毒罐里的吸附剂,可用来吸附氯气等有毒气体.如表列出了一定温度和压强下每立方厘米活性炭所能吸附的常见气体的体积.| 气 体 | 二氧化碳 | 氢气 | 氧气 | 氮气 | 氯气 |
| 气体相对分子质量 | 44 | 2 | 32 | 28 | 71 |
| 气体的沸点/℃ | -78 | -252 | -183 | -196 | -34 |
| 被吸附体积/mL | 97 | 4.5 | 35 | 11 | 494 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | 制备气体时,先装药品,后检查装置的气密性 | |
| B | 用试管加热时,先使试管底部均匀受热,后用酒精灯的外焰固定加热 | |
| C | 用量筒量取10mL液体时,先倒入接近10mL的液体,后用胶头滴管补至刻度线 | |
| D | 用托盘天平称量物质时,先加质量大的砝码,再加质量小的砝码,最后移动游码 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
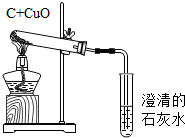 如图为用足量的木炭粉还原氧化铜的实验装置图,按要求回答:
如图为用足量的木炭粉还原氧化铜的实验装置图,按要求回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com