
分析 根据反应前后的质量差求出生成二氧化碳的质量,根据化学方程式可求得参加反应的碳酸钙的质量和生成的氯化钙的质量,进而求质量分数
解答 解:设参加反应的碳酸钙的质量为x,生成的氯化钙的质量为y,由题意可知,反应后生产二氧化碳12+100-107.6═4.4g
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
$\frac{100}{x}=\frac{111}{y}=\frac{44}{4.4g}$
x=10g,y=11.1g
由题意可知,反应后溶液的质量为107.6-(12-10)═105.6g
反应后氯化钙溶液中氯化钙的质量分数为:$\frac{11.1g}{105.6g}×100%$=10.5%
答:反应后氯化钙溶液中氯化钙的质量分数为10.5%.
点评 根据反应的化学方程式能表示反应中各物质的质量关系,由反应中某物质的质量可计算出反应中其它物质的质量.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:初中化学 来源: 题型:实验探究题
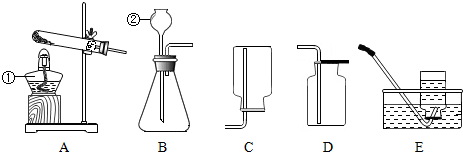
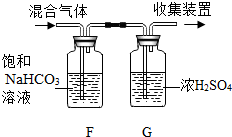
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是A、B两物质的溶解度曲线图,据图可知:
如图是A、B两物质的溶解度曲线图,据图可知:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
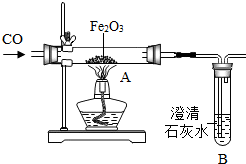 中国高铁在“一带一路”基础设施的互联互通中扮演着重要的角色.请结合所学知识回答相关问题:
中国高铁在“一带一路”基础设施的互联互通中扮演着重要的角色.请结合所学知识回答相关问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
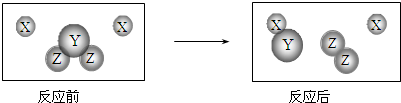
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com