
分析 固体溶解的速率与水的温度、固体颗粒大小、是否进行搅拌有关,然后选择一项进行实验分析.
解答 解:糖溶解的速率与温度和晶体颗粒大小有关,温度越高,溶解度增大,溶解越快;晶体颗粒越小,溶解越快;与是否搅拌也有关系,搅拌会加快糖的溶解速率.
故填:糖的颗粒大小;温度;
要验证搅拌对溶解速率的影响;可用烧杯取相同温度的水100mL,同时加入相同质量和颗粒大小蔗糖固体,用玻璃棒搅拌其中一个烧杯的水,并且开始计时,比较完全溶解所需要的时间.
故填:用烧杯取相同温度的水100mL,同时加入相同质量和颗粒大小蔗糖固体,用玻璃棒搅拌其中一个烧杯的水,并且开始计时,比较完全溶解所需要的时间.
点评 本题考查影响固体溶解速率的因素,要注意从不同角度进行分析.在设计实验时,要创设相同的条件改变溶解时的一个因素观察物质的溶解情况.


科目:初中化学 来源: 题型:解答题
| 编号 | 物质 | 杂质 | 确认物质含有杂质的实验操作 |
| ① | 二氧化碳 | 氢气 | |
| ② | 生石灰 | 石灰石 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
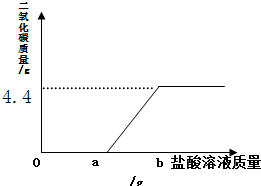 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 木炭在氧气中燃烧比在空气中燃烧旺,发出白光,并放出热量 | |
| B. | 铁丝在氧气中燃烧,火星四射,生成一种白色固体 | |
| C. | 把盛有红磷的燃烧匙伸人盛氧气的集气瓶中,产生大量白烟 | |
| D. | 硫在空气中燃烧产生淡蓝色火焰,生成二氧化硫气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入装有过氧化氢溶液的试管中 | 有少量气泡产生;木条不复燃 | 常温下过氧化氢溶液分解速率很慢. |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 有大量气泡产生;木条复燃 | 加入Al2O3,能加快过氧化氢溶液的分解速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com