


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:初中化学 来源: 题型:
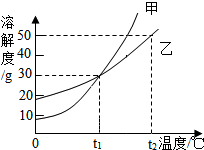
| A、t1℃时,甲和乙的溶解度均为30 |
| B、t1℃时,甲和乙的饱和溶液中溶质质量一定相等 |
| C、t2℃时,分别在100g水中各溶解20g甲、乙,降温后,乙溶液的溶质质量分数可能会大于甲溶液的溶质质量分数 |
| D、t2℃时,在100g水中放入60g乙,其溶质的质量分数为37.5% |
查看答案和解析>>
科目:初中化学 来源: 题型:
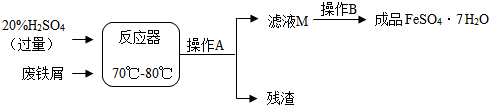
查看答案和解析>>
科目:初中化学 来源: 题型:
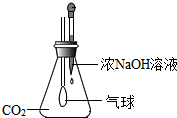 酸、碱、盐是重要的化合物,它们之间能发生复分解反应.
酸、碱、盐是重要的化合物,它们之间能发生复分解反应.| 实验操作 | 测定结果 | 溶液成分 |
| ①用pH试纸测定反应后溶液的酸碱度,操作方法是 | ②若pH>7 | |
| ③若 | NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:
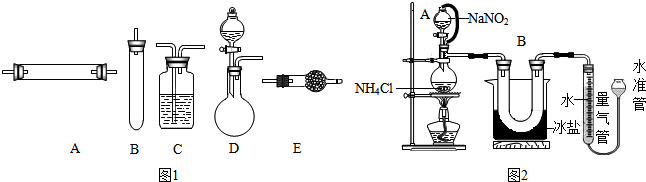
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
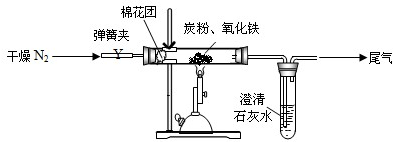
查看答案和解析>>
科目:初中化学 来源: 题型:
| 温度/℃ | FeSO4 | (NH4)2SO4 | xFeSO4?y(NH4)2SO4?zH2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
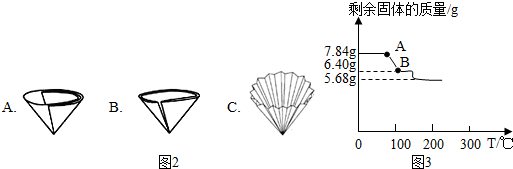
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com