
| 现象 | 结论和解释 | |
| ①取上述反应后的溶液,加入足量的CaCl2溶液 | 有白色沉淀生成 | 原溶液中有Na2CO3(填写化学式,下同) 反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl |
| ②将①所得的浑浊液过滤,向滤液中加入足量的稀盐酸 | 产生大量气泡 | 原溶液中有Na2CO3 |
| ③另取②中的滤液,滴入几滴酚酞溶液, | 溶液由无色变成浅红色 | 滤液显碱性 |
分析 【定性分析】根据题干信息来分析;
碳酸氢钠和氢氧化钠能够反应;
根据表中三种物质的不同性质分析实验现象和结论;
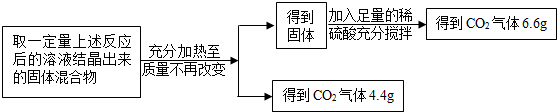
【定量分析】根据煅烧碳酸钙生成氧化钙以及碳酸钠与稀硫酸反应生成的二氧化碳的质量计算出碳酸钠的质量解答即可.
解答 解:【定性分析】当二氧化碳不足时,生成一部分碳酸钠,如适量完全生成碳酸钠,若过量则生成碳酸氢钠;故填:不足;
可能存在只有碳酸钠的情况;故填:碳酸钠;
因为NaHCO3+NaOH═Na2CO3+H2O,所以NaHCO3和NaOH不能共存;故填:否;
取一定量反应后溶液放入试管中,滴加适量的CaCl2溶液.有沉淀产生,说明含有氢氧化钠或碳酸钠,将步骤①所得的混合物过滤,洗涤,并将滤渣分成两部分,向其中一份步骤②所得固体中滴加稀盐酸,有气泡产生,说明沉淀中含有碳酸钙,则溶液中一定含有碳酸钠,若猜想①正确,取另一份步骤②所得溶液,滴加无色酚酞溶液,无色酚酞溶液变为红色,说明沉淀中含有氢氧化钙,则原溶液中含有氢氧化钠.
故答案为:
| 现象 | 结论和解释 | |
| ①取上述反应后的溶液,加入足量的CaCl2溶液 | 有白色沉淀生成 | 原溶液中有 Na2CO3(填写化学式,下同) 反应的化学方程式 Na2CO3+CaCl2=CaCO3↓+2NaCl |
| ②将①所得的浑浊液过滤,向滤液中加入足量的稀盐酸 | 产生大量气泡 | 原溶液中有 Na2CO3 |
| ③另取②中的滤液,滴入几滴酚酞溶液, | 溶液由无色变成浅红色 | 滤液显 碱性 |
点评 重点考查了碳酸氢钠、氢氧化钠及碳酸钠的性质、根据化学方程式的计算,在猜想反应后溶液中溶质时要考虑生成的可溶物及反应物的剩余情况.


科目:初中化学 来源: 题型:选择题
| A. | 铁生锈,铁在潮湿的空气中能生锈 | |
| B. | 氢气具有还原性,氢气能燃烧 | |
| C. | 铁具有银白色金属光泽,铁在干燥空气中不易生锈 | |
| D. | 硫在氧气中燃烧,加热时硫能熔化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 矿石名称 | 辉铜矿 | 孔雀石 | 黄铜矿 |
| 主要成分 | Cu2S | CuCO3•Cu(OH)2 | CuFeS2 |
| 溶解性 (20℃) | 离子 | OH- | Cl- | CO32- |
| Cu2+ | 不 | 溶 | 不 | |
| 有关反应 | CuCO3•Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O | |||
| CuCO3+2HCl═CuCl2+H2O+CO2↑ | ||||
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
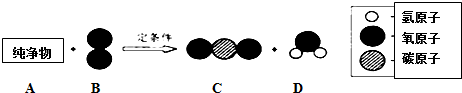
| A. | 生成C和D的分子个数比为3:4 | B. | 参加反应A的质量为44克 | ||
| C. | A中只含有碳元素和氢元素 | D. | 该反应为置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 碳酸氢钠常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的热稳定性进行探究.
碳酸氢钠常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的热稳定性进行探究.| 实验 | 实验现象 | 结论 |
| 实验一:取少量反应后的固体产物溶于水,滴入几滴酚酞试液 | 溶液变成红色 | 固体产物是NaOH,而不是Na2CO3 |
| 实验二:取少量反应后的固体产物溶于水,加入过量氯化钙溶液 | 产生白色沉淀 | 固体产物是Na2CO3,而不是NaOH |
| 实验三:取少量反应后的固体产物 , 加入过量稀盐酸 | 产生大量气泡 | 固体产物是Na2CO3,而不是NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在托盘上垫上纸并称取12 g NaOH固体 | |
| B. | 用100 mL量筒量取88 mL水 | |
| C. | 称量时发现指针向右偏转,应调节游码使天平平衡 | |
| D. | 把称取的NaOH固体直接倒入装有88 mL水的量筒中溶解 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com