
���� ��101.2g��CaCl2��HCl����Һ����μ���������������Ϊ10%��Na2CO3��Һʱ��̼�����Ⱥ�ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼�����ﵽa��ʱ��̼���ƺ�ϡ������ȫ��Ӧ������2.2g������̼��̼�����ٺ��Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ�����̼��Ƶ�������5.0g��
�Ȼ�����Һ�����ԣ�pH=7��ϡ���������ԣ�pH��7��
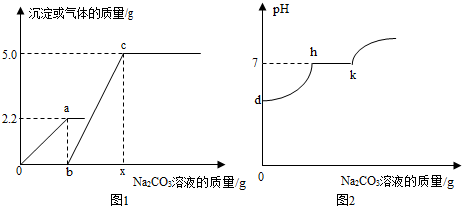
��� �⣺��ʵ��������ȡCO2�����Һ����к���̽��������101.2g��CaCl2��HCl����Һ����μ���������������Ϊ10%��Na2CO3��Һ��ʵ������м���Na2CO3��Һ�����������ɳ������������������ϵ��ͼ1��ʾ������Na2CO3��Һ����������Һ��pH�仯��ϵ��ͼ2��ʾ��
��1����b��ʱ����̼���Ƶ�����Ϊx�������Ȼ��Ƶ�����Ϊy��
Na2CO3+2HCl�T2NaCl+H2O+CO2����
106 117 44
x y 2.2g
$\frac{106}{x}$=$\frac{117}{y}$=$\frac{44}{2.2g}$��
x=5.3g��y=5.85g��
ͼ1��b������̼������Һ������Ϊ��5.3g��10%=53g��
��ͼ1��b���ֵΪ53��
��2����ͼ1��c��ʱ�����Ȼ��Ʒ�Ӧ��̼��������Ϊm�������Ȼ��Ƶ�����Ϊn��
Na2CO3+CaCl2�TCaCO3��+2NaCl��
106 100 117
m 5.0g n
$\frac{106}{m}$=$\frac{100}{5.0g}$=$\frac{117}{n}$��
m=5.3g��n=5.85g��
�ɣ�1���м����֪�����Ȼ��Ʒ�Ӧ���ĵ�̼������Һ��50g��
��Һ����Ϊ��101.2g+53g+53g-2.2g-5.0g=200g��
��Һ�е�������������Ϊ��$\frac{5.85g+5.85g}{200g}$��100%=5.85%��
����Һ�е�������������Ϊ5.85%��
��3��ͼ1��0��a�η�Ӧ�����У�ϡ����ϼ��٣�������ǿ��pH��С��7��ӽ�7�����������Һ��pH�仯�������ͼ2�е�d��h�����߱�ʾ��
���d��h��
���� 0��a��̼���ƺ�ϡ���ᷴӦ��b��c��̼���ƺ��Ȼ��Ʒ�Ӧ�����ǽ��Ĺؼ���Ҫע�����⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����֭pH=2 | B�� | ѩ��pH=4 | C�� | ʳ��ˮpH=7 | D�� | ����ˮpH=9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaNO3 Na2CO3 KCl | B�� | HCl NaOH MgCl2 | ||
| C�� | FeCl3 H2SO4 HCl | D�� | BaCl2 K2CO3 KNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ��ʵ | ���� |
| A | ˮ�;ƾ����ʱ�����С | ���Ӳ����˶� |
| B | ����Ӧ�ܷⱣ�� | ���ͷ��Ӽ����С |
| C | ����ˮ������ | ���Ƿ��Ӳ��˶� |
| D | ������Һ�ⶼ������ȼ�� | ��ͬ���ӵ������仯ѧ������ͬ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
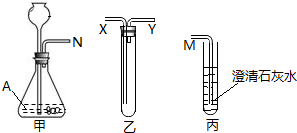
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ú�ˮ����ɹ�� | B�� | ��ľ̿ȼ����ȡů | ||
| C�� | �����Ƴ������� | D�� | ����˿�����ݵ�˿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������; | ���ʯ�и�� | ʯī���缫 |
| ��Ӧ���� | ��Ӳ�ȴ� | �ڵ����� |
| ��1g������ȫȼ�� | ����������̼����/g | �ų�����/kJ |
| ������ ��Ȼ�� | �������� 2.75 | �� 56 |
| �������� ú | �������� 3.67 | �� 32 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com