
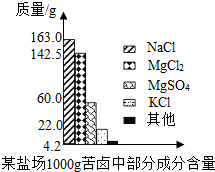
 海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.下图是我市某盐场苦卤中部分成分含量柱形图.试计算:
海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.下图是我市某盐场苦卤中部分成分含量柱形图.试计算:| 100g |
| 1000g |
| 95 |
| 14.25g |
| 80 |
| x |
| 58 |
| y |
| 100g |
| 1000g |
| 120 |
| 6g |
| 80 |
| z |
| 58 |
| w |
| ||
| 58 |
| 11.6g |
| 24 |
| m |
| 71 |
| n |


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:初中化学 来源: 题型:
 海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.如图是某盐场苦卤中部分成分含量柱形图.试计算:
海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.如图是某盐场苦卤中部分成分含量柱形图.试计算:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
海洋约占地球表面积的71%,具有十分巨大
的开发潜力。苦卤是海水提取食盐后的残液,利用
苦卤可以制得金属镁等化工原料。下图是我市某盐
场苦卤中部分成分含量柱形图。试计算:
(1) 若使100 g该苦卤中的MgCl2和MgSO4完全转化为Mg(OH)2沉淀,需要20% NaOH溶液多少克?
 (2)将上述沉淀完全转化为无水MgCl2,并在熔融状态下进行电解,可得金属镁多少克?氯气多少升(该条件下氯气密度为3.0 g/L)?
(2)将上述沉淀完全转化为无水MgCl2,并在熔融状态下进行电解,可得金属镁多少克?氯气多少升(该条件下氯气密度为3.0 g/L)?

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com