
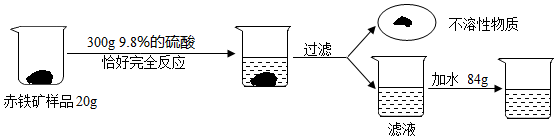
分析 (1)溶液稀释过程中时加入的水,所以溶质的质量保持不变,计算以此为依据.
(2)氧化铁和硫酸反应生成硫酸铁和水;
(3)(4)由于300g质量分数为9.8%%的硫酸完全反应,所以可以根据硫酸求算氧化铁的质量,最后求算出铁元素在样品中的质量分数;
(5)由于反应后的溶质为硫酸铁,所以要求算硫酸铁的质量,然后求算溶液中的硫酸铁的质量分数;
(6)冶炼过程铁元素是有损失,所以过程不能理解为铁元素守恒.
解答 解:溶液稀释过程中时加入的水,所以溶质的质量保持不变
设配制上述质量分数为9.8%的稀硫酸300g,需要质量分数为98%的浓硫酸的质量是a.
98%a=300g×9.8%
a=30g
设质量分数为9.8%的稀硫酸300g完全反应需要的氧化铁的质量为x,生成的硫酸铁的质量为y.
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
160 294 400
x 300g×9.8%=29.4g y
$\frac{160}{294}$=$\frac{x}{29.4g}$ x=16g
$\frac{294}{400}$=$\frac{29.4g}{y}$ y=40g
该赤铁矿样品中铁(不是氧化铁,要注意)的质量分数为$\frac{16g×\frac{56×2}{56×2+16×3}×100%}{20g}×100%$=56%
向过滤后所得滤液中加入84g水,则最终所得溶液(不饱和)中溶质的质量分数 $\frac{40g}{16g+300g+84g}×100%$=10%
设:现用250t此种赤铁矿炼制生铁,最终可炼得含铁90%的生铁样品的质量为140t,则炼制过程铁元素的转化率为m.
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
250t×$\frac{16g}{20g}×$100% m 140t×90%
$\frac{160}{112}$=$\frac{250t×\frac{16g}{20g}×100%m}{140t×90%}$
m=90%
炼制过程铁元素的损失率为1-90%=10%.
故答案为:(1)30;(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;(3)$\frac{160}{294}$=$\frac{x}{29.4g}$;(4)56%;(5)10%;(6)10%.
点评 本题有两点特别要注意,一是没必要按照给定的123456的顺序去逐一求算,而是要考虑在过程中哪些量需要求算,那些可以借助一个反应求算出来;第二是本题中最后一问有损失,在计算中尤其要注意,其实这就是化学问题的实际化,生产过程是每一个转化过程都有损失的.


 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:初中化学 来源: 题型:推断题
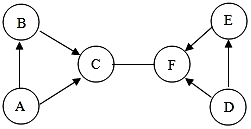 A、B、C、D、E、F是初中化学上册常见的物质,他们之间有如图所示的关系,图中短线“-”表示两端的物质能发生化学反应,箭头“→”表示物质间存在转化关系,部分反应物、生成物及反应条件均已略去,其中A、B组成元素相同,A是实验室制取氧气的一种药品,E、F组成元素相同,D是一种黑色固体,常温下很稳定,试推断:
A、B、C、D、E、F是初中化学上册常见的物质,他们之间有如图所示的关系,图中短线“-”表示两端的物质能发生化学反应,箭头“→”表示物质间存在转化关系,部分反应物、生成物及反应条件均已略去,其中A、B组成元素相同,A是实验室制取氧气的一种药品,E、F组成元素相同,D是一种黑色固体,常温下很稳定,试推断:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 物质 | A | B | C | D |
| 反应前(g) | 17 | 16 | 15 | 0 |
| 反应后(g) | 13 | X | 26 | Y |
| A. | 该项反应的A、B的质量比为1:1 | |
| B. | 该反应中X的值是16 | |
| C. | 该反应中Y的值是9 | |
| D. | 若A、B、C、D的相对分子质量分别为16、32、44、18,则该反应的化学方程式可表示为A+B=C+D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
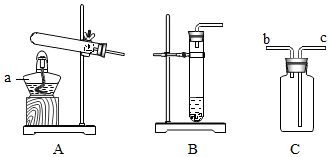 实验小组进行了如下实验.
实验小组进行了如下实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com