


| 实验操作 | 实验现象 | 实验结论 | |
| ① | 在尖嘴处点燃气体, 在火焰上方罩一个 .干燥、洁净的烧杯 |
烧杯内壁 .有无色液滴 |
混合气体中含有氢气 . |
| ② | 在火焰上方罩一个涂 .有少量石灰水的烧杯 |
烧杯内澄清 .石灰水变浑浊 |
混合气体中含有一氧化碳 . |


科目:初中化学 来源: 题型:阅读理解
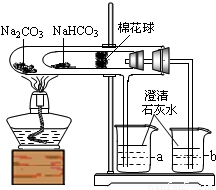
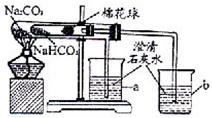 27、某化学兴趣小组的同学在学习了纯碱(Na2CO3)的性质后,联想到家中蒸制馒头时常用的物质小苏打(NaHCO3),于是采用市售的小苏打样品进行了如下实验探究.
27、某化学兴趣小组的同学在学习了纯碱(Na2CO3)的性质后,联想到家中蒸制馒头时常用的物质小苏打(NaHCO3),于是采用市售的小苏打样品进行了如下实验探究.查看答案和解析>>
科目:初中化学 来源: 题型:
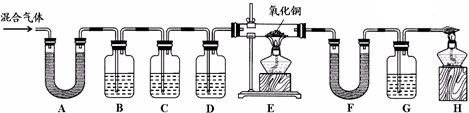
查看答案和解析>>
科目:初中化学 来源:江苏省模拟题 题型:实验题
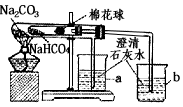
查看答案和解析>>
科目:初中化学 来源:镇江 题型:填空题
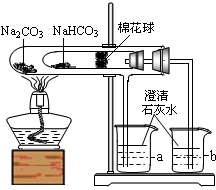
查看答案和解析>>
科目:初中化学 来源:2011年辽宁省大连市中考化学自适应练习(二)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com