
【题目】取10g锌粉和铜粉的混合物于烧杯中,向烧杯中分四次加入等质量的同种稀硫酸,实验过程中得到如下数据。
第1次 | 第2次 | 第3次 | 第4次 | |
加入稀硫酸的质量 | 20g | 20g | 20g | 20g |
剩余固体的质量 | 8.7g | 7.4g | 6.1g | 5.5g |
(1)混合物中铜粉的质量是________。
(2)所用稀硫酸中溶质的质量分数是_____。(保留计算过程)
【答案】5.5g 9.8%
【解析】
铜和硫酸不反应,锌和硫酸反应生成硫酸锌和氢气,每次加入的稀硫酸的质量相等,第1次加入20g稀硫酸固体减少了![]() ,说明20g稀硫酸恰好与1.3g锌反应,第四次加入20g稀硫酸固体减少了
,说明20g稀硫酸恰好与1.3g锌反应,第四次加入20g稀硫酸固体减少了![]() ,则混合物中的锌已经反应完,剩余固体的质量就是混合物中铜的质量,则混合物中铜的质量为5.5g。
,则混合物中的锌已经反应完,剩余固体的质量就是混合物中铜的质量,则混合物中铜的质量为5.5g。
(1)第1次加入20g稀硫酸固体减少了![]() ,说明20g稀硫酸恰好与1.3g锌反应,第四次加入20g稀硫酸固体减少了
,说明20g稀硫酸恰好与1.3g锌反应,第四次加入20g稀硫酸固体减少了![]() ,则混合物中的锌已经反应完,剩余固体的质量就是混合物中铜的质量,则混合物中铜的质量为5.5g。
,则混合物中的锌已经反应完,剩余固体的质量就是混合物中铜的质量,则混合物中铜的质量为5.5g。
(2)第一次加入20g稀硫酸固体减少了![]() ,则20g稀硫酸恰好与1.3g锌反应
,则20g稀硫酸恰好与1.3g锌反应
设第一次参加反应的硫酸的质量为x
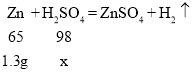
![]()
![]()
所用稀硫酸中溶质的质量分数是![]()
答:所用稀硫酸中溶质的质量分数是9.8%。


科目:初中化学 来源: 题型:
【题目】探究高锰酸钾的性质
(1)实验室用高锰酸钾制取氧气的化学方程式是______ 。为防止试管破裂,实验中采取的安全措施是______(写一点)。
(2)维生素C能使紫色高锰酸钾溶液褪色。常温下,利用如图实验测定苹果汁和橙汁中维生素C含量的相对多少,要得出正确结论,实验过程中需要进行控制的条件有______(填标号)。

A 烧杯中溶液的体积和浓度
B 胶头滴管每次吸取果汁的体积
C 两个胶头滴管滴出的每滴果汁的体积
(3)酸性KMnO4(相对分子质量为158)溶液可以测定居室内甲醛(CH2O)的含量是否超标(国家标准:成人允许的最高浓度为0.1mg/m3)。
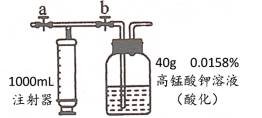
实验步骤如下:
①检查如图装置气密性良好。
②关闭止水夹______(填“a”或“b”,下同),打开______,用注射器抽取新装修的室内空气;接着关闭止水夹______,打开 ______,将气体全部推入酸性高锰酸钾溶液中。重复上述操作,至抽取到空气样品0.5m3与溶液中的高锰酸钾恰好完全反应。
③根据化学方程式计算:该居室内空气中含甲醛的浓度,写出计算过程。
(反应原理为4KMnO4 + 5CH2O + 6H2SO4 == 2K2SO4 + 4MnSO4 + 5CO2 + 11H2O。)
由此判断该居室内甲醛含量______(填“有”或“没有”)超标。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室中现有一固体混合物A,其中可能含有 Na2CO3、BaSO4、NaC1、CuO四种物质中的两种或多种。按如图所示进行实验,出现的现象如图中所述。(设过程中所有可能发生的反应都恰好完全进行)
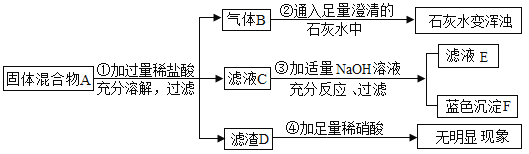
试根据实验过程和发生的现象判断
(1)产生的气体B的化学式是___。
(2)写出步骤③中生成蓝色沉淀F的化学反应方程式___。
(3)在溶液C中,一定大量存在的酸根离子是___。
(4)混合物A中,还不能确定存在的物质是___(写化学式),要进一步确定其是否存在,可用固体混合物A的样品进行再实验,请简要说明实验操作步骤、发生的现象及结论:___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对面粉厂悬挂“禁止明火”的宣传感到不解。了解到面粉的主成分是淀粉,属于易燃易爆物,完全燃烧产物为CO2和H2O,为了进一步探究面粉的组成,该小组同学设计了以下实验。
(提出问题)面粉主要由哪些元素组成?
(作出猜想)小明猜想:面粉中一定含有C、H元素,他作出此猜想的依据是:_______
小红猜想:面粉中一定含有C、H、O三种元素。
小文认为小红的猜想错误,因为面粉中是否含有氧元素需要实验验证。
(设计实验)兴趣小组的同学们设计如图所示的实验。
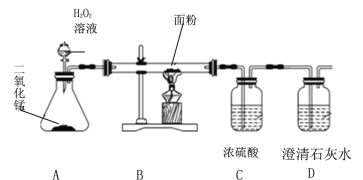
(1)A装置中二氧化锰的作用是___________,发生反应的化学方程式为____________。
(2)打开分液漏斗通入氧气,点燃B处酒精灯。实验现象和结论如下:
实验现象 | 实验结论 |
_______ | ①面粉中含有碳元素 |
B装置硬质玻璃管内壁有水珠出现 | ②面粉中含有氢元素 |
(拓展交流)有同学认为结论②不正确,请说明原因_______
(分析判断)兴趣小组的同学们取面粉8.1 g,使其完全燃烧后测得生成二氧化碳的质量为13.2 g,生成水的质量为4.5 g,由此可以判断出面粉中________(填“含”或“不含”)氧元素。
(反思交流)通过对上述实验分析,为避免事故发生,面粉在生产、运输过程可采取的措施有___。
A 密封门窗,隔绝空气
B 严禁吸烟,杜绝火源
C 轻拿轻放,减少扬尘
D 提高面粉的着火点
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用氯酸钾和二氧化锰的混合物制取氧气,混合物的质量变化如右图,下列分析不正确的是( )
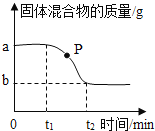
A. 反应结束时最多能收集到(a-b)g氧气
B. P点处固体成分是氯酸钾和氯化钾
C. 在反应过程中氯元素的质量分数不断增大
D. 在0~t2时段,MnO2在混合物中的质量不断增多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】回答下列与金属有关的问题。
(1)超细铁微粒是一种纳米型材料,可在低温下将CO2分解为碳单质。下列推测中,不合理的是_____:
A 超细铁微粒在反应中可能作催化剂
B 该反应的另一产物可能是O2
C 该反应属于化合反应
D 该反应有助于减少CO2气体排放
(2)金属镁能在CO2气体中燃烧:2Mg+CO2![]() 2MgO+C,该反应中的还原剂是_____;
2MgO+C,该反应中的还原剂是_____;
(3)向FeSO4和CuSO4的混合溶液中加入一定量的锌粉,充分反应后过滤,得到固体A和滤液,将A放入少量稀H2SO4中有气体产生。综合分析实验过程可知,固体A中可能含有的物质是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某反应的微观示意图,回答问题。
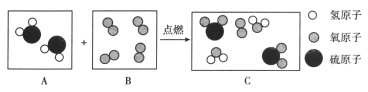
(1)A框中物质属于纯净物中的______________(选填“单质”或“化合物”)。
(2)保持B框中物质化学性质的最小粒子是 ______________。
(3)从上述反应能得出化学变化的微观本质是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸铜的制备如图为某兴趣小组用含较多杂质的铜粉制取硫酸铜晶体[CuSO45H2O]的两种实验方案。
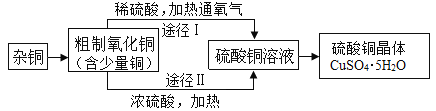
(1)制备中需过滤得到硫酸铜晶体。过滤时需要的玻璃仪器有烧杯、玻璃棒和______。
(2)灼烧杂铜除去其中的杂质,产生CO2和少量CO.灼烧后的产物为CuO及少量Cu.产物中含有Cu的可能原因是______(填序号)。
A灼烧过程中,部分氧化铜与一氧化碳反应
B灼烧不充分,铜未被完全氧化
C该条件下铜无法被氧气氧化
(3)方案Ⅰ通入氧气,少量Cu转化为CuSO4.该反应的化学方程式为______。
(4)方案Ⅱ中加入浓硫酸发生的反应有Cu+2H2SO4=CuSO4+SO2↑+2H2O
方案Ⅰ优于方案Ⅱ的理由是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲和乙两种物质的溶解度曲线。
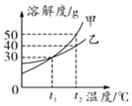
(1)t1℃时,将18g乙加入50g水中充分溶解,所得溶液为_____溶液。(填“饱和”或“不饱和”)
(2)t2℃时用相同质量的水配制甲和乙的饱和溶液,所需溶质质量的关系为甲_____乙。
(3)取t2℃时甲的饱和溶液90g,稀释为溶质质量分数为10%的溶液,需要加水的质量为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com