
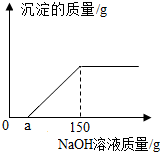
 现有8g Fe2O3和CuO的混合物,进行如下实验:把混合物全部加入到50克足量的硫酸溶液中,完全溶解后,滴加溶质质量分数为8%的氢氧化钠溶液,滴加氢氧化钠溶液的质量与生成沉淀质量的关系如图所示.回答下列问题:
现有8g Fe2O3和CuO的混合物,进行如下实验:把混合物全部加入到50克足量的硫酸溶液中,完全溶解后,滴加溶质质量分数为8%的氢氧化钠溶液,滴加氢氧化钠溶液的质量与生成沉淀质量的关系如图所示.回答下列问题:分析 (1)根据氢氧化钠和硫酸反应生成硫酸钠和水,依据氢氧化钠的质量计算参加反应的硫酸的质量;
(2)根据假设8g铁全部是氧化铜或氧化铁,然后计算a的值,结合题意进行分析;
(3)根据a的质量和氢氧化钠与硫酸反应的关系式,进行计算和分析.
解答 解:(1)设硫酸的质量分数为x
2NaOH-----Na2SO4-----H2SO4
80 98
150g×8% 50g×x
$\frac{80}{150g×8%}$=$\frac{98}{50g×x}$
x=29.4%;
(2)若8克固体全部为Fe2O3,则将铁元素全部转化为沉淀所需氢氧化钠溶液的质量为(y1)
Fe2O3----2Fe(OH)3----6NaOH
160 240
8g y1×8%
$\frac{160}{8g}$=$\frac{240}{{y}_{1}×8%}$
y1=150g
所以a=0
同理可得,当8克固体全部为CuO时,y2=100g
所以a=50
所以a的取值范围:0<a<50;
(3)若a=30,则与氢氧化钠反应的硫酸溶液量为
2NaOH-----H2SO4
80 98
30g×8% y3×29.4%
$\frac{80}{30g×8%}$=$\frac{98}{{y}_{3}×29.4%}$
y3=10g
则溶解氧化物固体的硫酸量为(50-10)×29.4%,这些硫酸能夺取的氧元素为
16×40×29.4%÷98=1.92g
剩余固体的量为(8-1.92)×2=12.16g.
故答案为:(1)29.4%;
(2)0<a<50;
(3)12.16g.
点评 本题是数形结合类问题,分析反应的关系图是正确判断反应进行的依据和基础,弄清折点的含义,是解决此题的关键之所在.


科目:初中化学 来源: 题型:选择题
| A. | K2SO4 BaCl2 NaNO3 NaCl | B. | HCl Na2CO3 BaCl2 Na2SO4 | ||
| C. | KOH Na2SO4 CuSO4 NaCl | D. | KCl AgNO3 KNO3 NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验的步骤为计算、称取、量取、溶解、装瓶存放 | |
| B. | 溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率 | |
| C. | 把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签 | |
| D. | 量取水时,用规格为50mL的量筒量取42.5mL蒸馏水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 红枣包装中常使用一种袋装防腐剂,品名为“504双 吸剂”,其标签如图所示. 同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双 吸剂”,其标签如图所示. 同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com