
老师在讲解溶洞的形成时,告诉了同学们一个新的化学反应:
CaCO3+CO2+H2O=Ca(HCO3)2
化学兴趣小组的同学们提出一个大胆的猜想:“Na2CO3溶液也能与CO2发生反应”.
为了确定同学们的猜想是否正确,兴趣小组在老师的指导下,通过实验探究的方法,完成了对该猜想的判断.请你完成兴趣小组在实验探究活动中的部分实验报告.
【实验目的】:探究Na2CO3溶液能否与CO2反应
【实验药品】:大理石、CaO、Na2CO3溶液、饱和的NaHCO3溶液、CaCl2溶液、浓盐酸、稀硫酸、浓硫酸、澄清石灰水
【查阅资料】:
①2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O;
②Na2CO3+CaCl2═CaCO3↓+2NaCl
③2NaHCO3+CaCl2═CaCO3↓+2NaCl+H2O+CO2↑
④二氧化碳能溶于水,但几乎不溶于饱和NaHCO3溶液
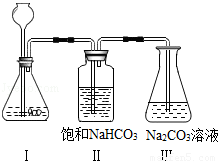
【实验装置】:如图
【实验操作步骤与现象】:
①制取二氧化碳时应选用上述的 (请从以上给出的药品中选择并填药品的名称)
②装置Ⅱ中盛放的饱和NaHCO3溶液的作用是 .
③使过量的CO2通过装置Ш,充分反应后,将其中所得的溶液取出3mL于试管中,然后向试管中加入 试剂(请从以上给出的药品中选择并填药品的名称)
a.当试管中 现象时,Na2CO3溶液与CO2没有发生反应;
b.当试管中 现象时,Na2CO3溶液与CO2发生了化学反应,其反应的化学方程式为 .
【结论】:通过实验探究,同学们的猜想是正确的.
①大理石和浓盐酸;②除去混入的氯化氢气体;③CaCl2;a、有沉淀生成; b、既有气体又有沉淀生成;Na2CO3+CO2+H2O═2NaHCO3
【解析】
试题分析:①制取二氧化碳可用药品是大理石与浓盐酸;②浓盐酸易挥发,用浓盐酸制取的二氧化碳中混有氯化氢气体,饱和的NaHCO3溶液与氯化氢气体可反应,除去氯化氢气体,防止进入Ⅲ与碳酸钠溶液反应,影响实验进行;③由题意可知:氢氧化钙与碳酸钠溶液和碳酸氢钠溶液都能反应生成沉淀,现象相同,无法鉴别,所以选择氯化钙;碳酸钠与氯化钙反应生成碳酸钙沉淀,碳酸氢钠与氯化钙溶液反应生成碳酸钙沉淀、氯化钠、水和二氧化碳,所以可以根据是否生成气体进行区分碳酸钠溶液和碳酸氢钠溶液;由CaCO3+CO2+H2O=Ca(HCO3)2可知,Na2CO3溶液与CO2发生化学反应的化学方程式是:Na2CO3+CO2+H2O═2NaHCO3;
考点:实验探究物质的性质或变化规律.


科目:初中化学 来源: 题型:阅读理解
 (2013?密云县一模)老师在讲解溶洞的形成时,告诉了同学们一个新的化学反应:CaCO3+CO2+H2O=Ca(HCO3)2
(2013?密云县一模)老师在讲解溶洞的形成时,告诉了同学们一个新的化学反应:CaCO3+CO2+H2O=Ca(HCO3)2查看答案和解析>>
科目:初中化学 来源:2013年北京市密云县中考化学一模试卷(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com