
【题目】下列四个图象能正确反映对应变化关系的是( )
A.在密闭容器中用红磷测定空气中氧气的含量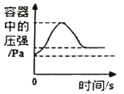
B.向盛有二氧化锰的烧杯中不断加入过氧化氢溶液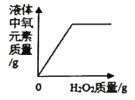
C.等质量氯酸钾制氧气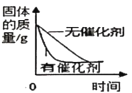
D.加热高锰酸钾制取氧气时剩余物的质量
科目:初中化学 来源: 题型:
【题目】某厂采用臭氧氧化—钙法吸收工艺对锅炉烟气(含N2、空气、NO、SO2等)进行同时脱硫(SO2)脱硝(NOx)处理,减少了设备建设用地,下图为主要吸收装置——鼓泡反应器。请回答:
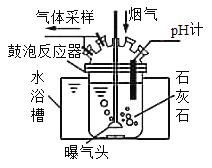
(1)NO和O3反应产物除生成NO2外,还生成能使带火星木条复燃的气体,反应的化学方程式为____,属于____反应(填基本反应类型)。
(2)鼓泡反应器中SO2和石灰水反应生成CaSO3和水,反应的化学方程式____。
(3)鼓泡反应器放在水浴槽中,控制温度35℃,水浴加热的优点是____。曝气头为半球形,作用是____。
(4)下图是同时脱硫(SO2)脱硝(NOx)与单独脱硫、脱硝去除率的对比图。
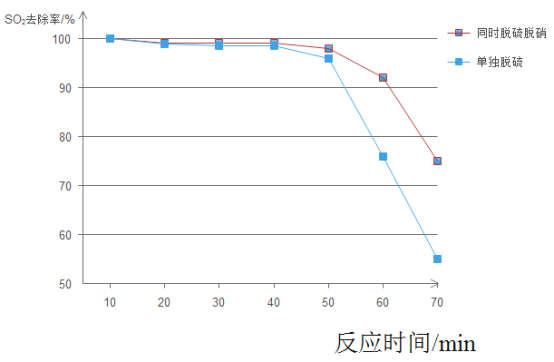
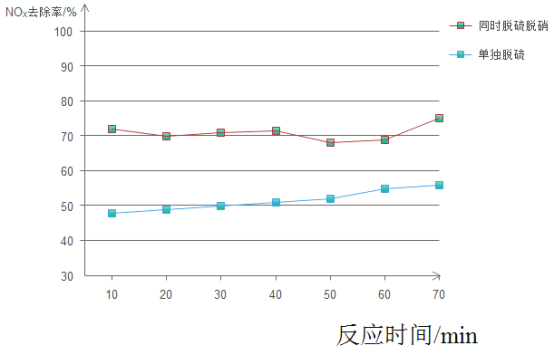
①分析图像,你认为同时脱硫脱硝在工业生产中的优势是____、____。
②左图中,50min后SO2去除率明显降低的原因可能是____。
(5)计算单独脱硫时,1吨质量分数为0.15%的石灰水理论上可吸收SO2气体的质量是___克?(精确到小数点后一位)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下4个图象,能正确反映对应关系的是( )
A | B | C | D |
加热一定质量的高锰酸钾固体 | 镁条在空气中燃烧 | 木炭在盛有氧气的密闭容器内燃烧 | 电解水生成两种气体 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】偏二甲肼(C2H8N2)与N2O4反应放出的能量能把火箭送入太空。该化学方程式为C2H8N2+2N2O4=2X↑+3N2↑+4H2O↑,下列说法正确的是()
A.X的化学式为CO
B.偏二甲肼(C2H8N2)中碳、氢、氮元素的质量比为1:4:1
C.该反应属于分解反应
D.偏二甲肼中碳的质量分数为40%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用下图表示:
![]()
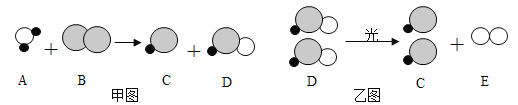
(1)乙图所示反应的基本反应类型为_________反应(填“化合”或“分解”);
(2)上述物质中,D属于___________(填“单质”或“化合物”);
(3)以甲图为例分析,你能总结出的一条结论是:____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组的同学为了测定实验室中高锰酸钾样品的纯度,取20g该样品,依次加热该混合物,t1、t2、t3、t4时间后,称得剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量(g) | 19.88 | 19.56 | 19.36 | 19.36 |
试计算:(1)加热__________时间后高锰酸钾已经完全反应。
(2)完全反应后产生氧气的质量为_________g。
(3)求该样品中高锰酸钾的质量分数_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组为探究铁、铜、锰(Mn)、银的金属活动性顺序,进行了如下三个实验(其中金属均已打磨,且形状、大小相同,试管中所用溶液的体积相同)。下列判断不正确的是
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
实验现象 | 立即产生气泡,速率较慢 | 立即产生气泡,速率较快 | 铜片的表面有银白色固体,一段时间后。溶液由无色变为蓝色 |
A.通过实验一和实验二的反 应剧烈程度,能判断出铁和锰的金属活动性强弱
B.在上述三个实验基础上再增加一个铜和5%盐酸的实验,则能判断出四种金属的活动性顺序
C.通过上述三个实验,能判断出四种金属的活动性顺序
D.通过实验三的反应现象,能判断出铜和银的金属活动性强弱
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】价类二维图反映的是元素化合价与物质类别之间的关系,构建价类二维图是化学学习的重要方法。下图是某同学绘制的关于碳元素的价类二维图。
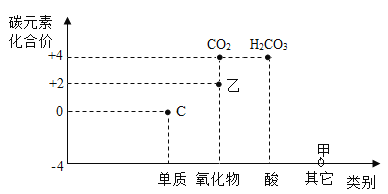
(1) 甲为天然气的主要成分,其化学式为_____。
(2) 根据碳元素的价类二维图完成下表:
物质之间的反应或转化 | 碳元素化合价的变化情况 | 化学方程式 |
CO2→H2CO3 | 不变 | ①_____ |
C→乙 | 升高 | ②_____ |
C和CO2反应 | ③_____ | C+ CO2 |
(3)以CO2为原料,与H2经催化可转化为A物质,反应原理如下图所示:
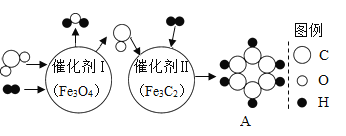
①写出A的化学式_____。
②在催化剂Ⅰ(Fe3O4)作用下发生反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁(Fe2O3)粉末中的一种或两种。同学们对该粉末进行了研究。
(1)
实验方案 | 实验现象 | 实验结论 |
取少量红色粉末放入试管中,滴加足量的稀盐酸振荡 | 红色粉末全部消失,溶液呈棕黄色 | 粉末为Fe2O3 |
粉末为Cu |
写出“红色粉末全部消失”发生反应的化学方程式_______。
(2)取该粉末放入硬质玻璃管中,先通CO,然后再用酒精喷灯加热一段时间,停止加热继续通入CO至装置冷却。实验装置如图:
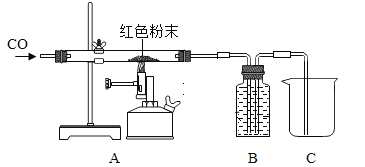
①实验时,先通CO再加热的目的是_________。
②若该粉末全部是氧化铁,在硬质玻璃管中观察到的实验现象是_________。B装置是用于吸收二氧化碳并收集CO,其中盛放的试剂最好是__________。
A NaOH 溶液 B 稀盐酸 C 水
③如果该实验没有装置B、C,实验造成的危害是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com