【答案】
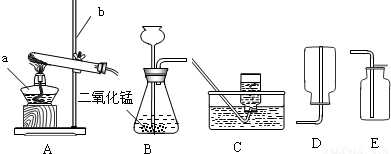
分析:(1)如图所示制取氧气的装置,写出常用仪器;
(2)用高锰酸钾制取氧气时,正确书写文字表达式为高锰酸钾

锰酸钾+二氧化锰+氧气;
(3)常用氯化铵固体与碱石灰固体混和加热来制取氨气;常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.制取并收集氨气,选择A、D;
(4)检验氧气是否集满的方法是用带火星的木条伸到集气瓶口,看是否复燃;
(5)根据氧气的性质,用排气法或排水法,来选择收集氧气的导气管的方向;
(6)①用双氧水和二氧化锰来制取氧气时,不需要加热,性质B装置;②从表中数据可分析知,MnO
2的用量对反应速率有影响;
③过氧化氢(H
2O
2)溶液的浓度对反应速率有影响,设计方案:双氧水溶液的溶质质量分数越大,反应越快.每次均取5mL30%的双氧水溶液,然后稀释成不同溶质质量分数的溶液进行实验,记录时间.
解答:解:(1)如图所示制取氧气的装置,写出常用仪器,故答:酒精灯、铁架台;
(2)用高锰酸钾制取氧气时,正确书写文字表达式;
(3)①根据:常用氯化铵固体与碱石灰固体混和加热来制取氨气,反应装置选择A;
②根据:常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,收集装置选择D;
(4)检验氧气是否集满的方法是用带火星的木条伸到集气瓶口,看是否复燃;
(5)根据氧气的性质,其密度大于空气,故用排气法从b口进入;因为氧气难溶于水,故若将装置中充满水,则O
2由a口进入.
(6)①有影响.在一定范围内,MnO
2的用量越大,反应越快; ②有影响.双氧水溶液的溶质质量分数越大,反应越快.每次均取5mL30%的双氧水溶液,然后稀释成不同溶质质量分数的溶液进行实验.记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
实验次序 1 2 3 4 5 6 7 8
双氧水溶液溶质质量分数 1% 3% 5% 10% 15% 20% 25% 30%
MnO
2粉末用量(克) 0.2 0.2 0.2 0.2 0.2 0.2 0.2 0.2
收集同样气体所用时间(秒)660 220 205 80 25 9 4 3
故答为:(1)酒精灯、铁架台;(2)高锰酸钾

锰酸钾+二氧化锰+氧气;(3)A、D;(4)用带火星的木条伸到集气瓶口,看是否复燃;(5)b、a;(6)B;双氧水
水+氧气;①有,②有;每次均取5mL30%的双氧水溶液,然后稀释成不同溶质质量分数的溶液进行实验,记录时间.
点评:学会比较用高锰酸钾和用过氧化氢溶液和二氧化锰制取氧气的区别;掌握制取氧气的反应原理、制法及操作步骤和注意点,了解氧气的收集、检验和验满方法.

 锰酸钾+二氧化锰+氧气;
锰酸钾+二氧化锰+氧气; 锰酸钾+二氧化锰+氧气;(3)A、D;(4)用带火星的木条伸到集气瓶口,看是否复燃;(5)b、a;(6)B;双氧水
锰酸钾+二氧化锰+氧气;(3)A、D;(4)用带火星的木条伸到集气瓶口,看是否复燃;(5)b、a;(6)B;双氧水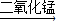 水+氧气;①有,②有;每次均取5mL30%的双氧水溶液,然后稀释成不同溶质质量分数的溶液进行实验,记录时间.
水+氧气;①有,②有;每次均取5mL30%的双氧水溶液,然后稀释成不同溶质质量分数的溶液进行实验,记录时间.

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
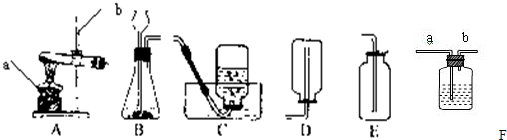
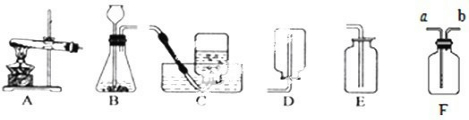

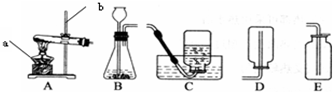 实验室常用下列装置来制取氧气:
实验室常用下列装置来制取氧气: