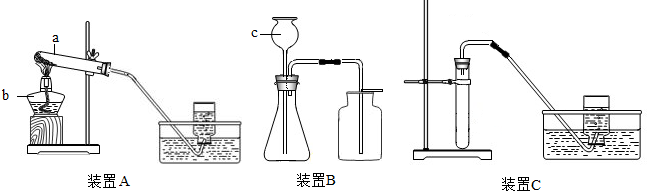
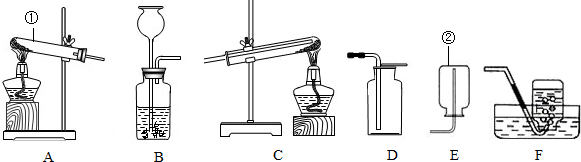
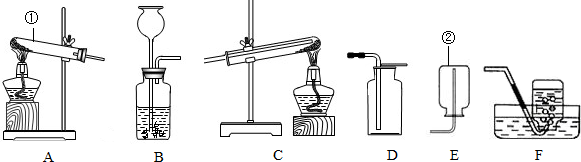
解:(1)仪器①为发生装置中用作反应容器的试管,仪器②为收集装置中用于收集气体的集气瓶;
(2)加热分解高锰酸钾制取氧气,选用的药品为固体高锰酸钾、反应条件为加热,因此应选用可用于对固体加热的装置A作为发生装置;由于氧气密度比空气大,应采用向上排空气法收集,而装置E为向下排空气,因此收集氧气时不选用此装置;采用F装置进行排水集气法收集氧气时,为防止停止加热后水槽内的水倒流入试管而使试管出现炸裂,因此在收集完毕时应先将导管从水中移出然后熄灭酒精灯;当采取向上排空气收集满氧气时,氧气从集气瓶口逸出,放在瓶口的带火星的木条则会复燃,因此通常采取将带火星木条放在瓶口,观察到木条复燃可说明氧气已经收集满;
(3)用过氧化氢溶液与二氧化锰混合制取氧气,所选择用药品为固体与液体反应且不需要加热,因此应选用发生装置B作为制取氧气的发生装置;在二氧化锰催化下过氧化氢分解生成水和氧气,反应的化学方程式为2H
2O
2
2H
2O+O
2↑;反应前后二氧化锰的质量及其化学性质均不变,为反应的催化剂;因此,该反应为一种物质过氧化氢反应生成水和氧气两种物质,反应符合“一变多”的分解反应的特点,该反应为分解反应;
故答案为:
(1)①试管;②集气瓶;
(2)A;E;氧气密度比空气大;移出导管;熄灭酒精灯;防止水回流至试管而使试管炸裂;用带火星的木条放在瓶口,木条复燃,氧气收集满;
(3)B;2H
2O
2
2H
2O+O
2↑;催化;分解反应.
分析:(1)根据装置图中仪器的图示,写出指定仪器的名称;
(2)根据加热高锰酸钾制取氧气时所使用药品的状态及反应的条件,确定制取时的发生装置;结合氧气的密度特点,说明不能用于收集氧气的收集装置的原因;根据对操作要求的理解,说明使用排水法收集完气体后的操作先后顺序并解释原因;利用氧气能使带火星木条复燃的特性,设计验满氧气的方法;
(3)根据利用过氧化氢在二氧化锰催化下制取氧气时所使用药品的状态与反应条件,确定此时所应选用的发生装置,并写出反应的化学方程式;根据反应中二氧化锰的特点,判断反应中二氧化锰的作用;最后,根据反应中物质种类特点,判断反应所属的基本类型.
点评:本题为重点实验气体的制取的再现式考查,考查中侧重于对实验的装置、操作等的理解,此部分知识为必考知识,应做到熟练掌握.

 2H2O+O2↑;反应前后二氧化锰的质量及其化学性质均不变,为反应的催化剂;因此,该反应为一种物质过氧化氢反应生成水和氧气两种物质,反应符合“一变多”的分解反应的特点,该反应为分解反应;
2H2O+O2↑;反应前后二氧化锰的质量及其化学性质均不变,为反应的催化剂;因此,该反应为一种物质过氧化氢反应生成水和氧气两种物质,反应符合“一变多”的分解反应的特点,该反应为分解反应; 2H2O+O2↑;催化;分解反应.
2H2O+O2↑;催化;分解反应.

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案