
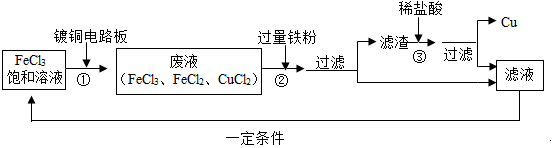
分析 根据给定的图表分析对应的物质之间的转化关系,进而理解对应的化学反应.
解答 解:过程①是过量的氯化铁和铜反应,生成了氯化亚铁和氯化铜,同时剩余氯化铁;
过程②是加入过量铁粉,此时氯化铁和氯化铜都能和铁反应,生成氯化亚铁和铜,还剩余铁,所以过滤得到的滤渣为铜和铁;
过程③滤渣为铁和铜的混合物,加入稀盐酸,只有铁和盐酸反应生成氯化亚铁和氢气,过滤得到铜单质和氯化亚铁溶液.
所以(1)步骤②中发生了两个反应:Fe+2FeCl3═3FeCl2和 Fe+CuCl2=FeCl2+Cu;
(2)滤渣的成分是铁和铜;
(3)最后得到的溶液中有剩余的氯化铁和生成的氯化亚铁,以及生成的铜.所以该流程中可以循环、回收利用的物质是铜和氯化铁或者氯化亚铁.
故答案为:
(1)Fe+CuCl2=FeCl2+Cu;
(2)铁和铜;
(3)铜和氯化铁或者氯化亚铁.
点评 归纳类的题目解答不要从题干区分析解答,而是先研究需要回答的问题,从问题去寻找题干中解答可能用到的信息和线索.


科目:初中化学 来源: 题型:选择题
| 选项 | 待鉴别的物质 | 鉴别方法 |
| A | 水、过氧化氢溶液 | 加二氧化锰,观察能否产生气体 |
| B | 硝酸铵和氢氧化钠 | 加水溶解,用手触摸烧杯外壁温度的变化 |
| C | NaOH与Na2CO3 | 滴加酚酞溶液,观察溶液颜色的变化 |
| D | 棉纤维、羊毛纤维 | 点燃,闻燃烧产生的气味 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 含有可溶性钙、镁化合物的水是硬水 | |
| B. | 温度升高或压强增大时,气体在水中的溶解度均增大 | |
| C. | 用铅锑合金制作保险丝,是因为熔点低 | |
| D. | 混有泥沙的天然水通过加明矾吸附、过滤、蒸馏、消毒杀菌,可净化为生活用的自来水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯化钠和亚硝酸钠都有咸味,都可用做调味品 | |
| B. | 氢氧化钠溶液、浓硫酸、氧化钙都能干燥氢气 | |
| C. | 试管内壁附着铜、氧化铁、氢氧化铜时都可以用稀盐酸除去 | |
| D. | 氢氧化钠、碳酸钠的溶液都显碱性的原因是溶液中都含有大量OH- |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金属元素:水银、钙、金、铝 | B. | 合成材料:聚乙烯、尼龙、铝合金 | ||
| C. | 混合物:冰水共存物、酒精、熟石灰 | D. | 氧化物:氧气、氯酸钾、生石灰 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验次数 | 1 | 3 | 4 | 5 | 6 |
| 取样品质量(g) | 31.0 | 31.0 | 31.0 | 31.0 | 31.0 |
| 取稀硫酸质量(g) | 30.0 | 90.0 | 120.0 | 150.0 | 180.0 |
| 产生气体质量(g) | 0 | a | 0.3 | 0.5 | 0.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com