
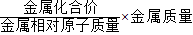 ”求得;
”求得;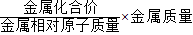
 ≈0.18g<0.2g,则该锌粉中的甲应该是能与酸反应放出氢气的金属,且同等质量的金属甲完全反应产生氢气质量大于锌;而A、D选项中铜、银不能与酸反应产生氢气,故A、D不正确;而等质量的铁、镁与酸完全反应放出氢气的质量都比锌大,因此,B、C选项都有可能是正确的;
≈0.18g<0.2g,则该锌粉中的甲应该是能与酸反应放出氢气的金属,且同等质量的金属甲完全反应产生氢气质量大于锌;而A、D选项中铜、银不能与酸反应产生氢气,故A、D不正确;而等质量的铁、镁与酸完全反应放出氢气的质量都比锌大,因此,B、C选项都有可能是正确的; ≈0.21g>0.2g,则铁粉中金属乙不能与酸反应或虽是能与酸反应放出氢气但等质量的金属乙完全反应放出氢气的质量小于铁;而选项B中等质量的镁完全反应放出氢气的质量大于铁,故B选项不正确;选项C中的乙的铜不能与酸反应,铁粉中混有铜时放出氢气的质量偏小,故C选项正确;
≈0.21g>0.2g,则铁粉中金属乙不能与酸反应或虽是能与酸反应放出氢气但等质量的金属乙完全反应放出氢气的质量小于铁;而选项B中等质量的镁完全反应放出氢气的质量大于铁,故B选项不正确;选项C中的乙的铜不能与酸反应,铁粉中混有铜时放出氢气的质量偏小,故C选项正确;

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:初中化学 来源: 题型:
| A、甲为Cu、乙为Zn | B、甲为Fe、乙为Mg | C、甲为Mg、乙为Cu | D、甲为Ag、乙为Al |
查看答案和解析>>
科目:初中化学 来源:松江区二模 题型:单选题
| A.甲为Cu、乙为Zn | B.甲为Fe、乙为Mg |
| C.甲为Mg、乙为Cu | D.甲为Ag、乙为Al |
查看答案和解析>>
科目:初中化学 来源:2011年湖南省永州市道县四马桥中学中考化学模拟试卷(解析版) 题型:选择题
查看答案和解析>>
科目:初中化学 来源:2003年上海市松江区中考化学二模试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com