
【题目】向AgNO3溶液中加入过量的铜粉充分反应,回答下列问题:
(1)AgNO3溶液中存在的离子有____.
(2)图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):![]() ____、
____、![]() ____.
____.
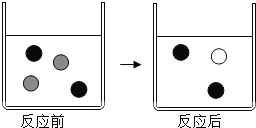
(3)该反应的化学方程式为_____,1个铜原子完全反应生成____个银原子.
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:初中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予了在锂离子电池发展上做出突出贡献的三位杰出科学家。在锂离子电池中常用到磷酸亚铁锂(LiFePO4)作为优质正极材料。
(1)锂离子(Li+)属于_________(填“阴”或“阳”)离子。图一x的数值是______,图二中与锂原子的化学性质相似的粒子是______(填序号)。

(2)已知磷酸亚铁锂中锂元素显+1价,则磷元素显______价。
(3)在工业上制备磷酸亚铁锂时常发生如下反应:2LiH2PO4+Fe2O3+C![]() 2LiFePO4+2X+CO 根据质量守恒定律,则其中X的化学式是________。
2LiFePO4+2X+CO 根据质量守恒定律,则其中X的化学式是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中错误的是( )
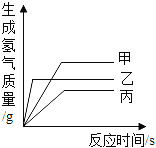
A. 金属活动性:乙>甲>丙 B. 生成氢气的质量:甲>乙>丙
C. 相对原子质量:乙>丙>甲 D. 消耗硫酸的质量:甲>乙>丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)在分子、原子、原子核、质子、中子、电子等粒子中,找出符合下列条件的粒子填在相应的横线上:
(1)化学变化中的最小粒子是________。
(2)带正电荷的粒子是___ _。
(3)不显电性的粒子是_ __。
(4)决定原子质量大小的粒子主要是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用红磷测量空气中氧气含量实验,在实际操作中,并不容易成功,理由是_____。正常空气中的各成分按体积计,由多到少的顺序是,_____(要求:写完整,且顺序完全正确)。医生建议吸氧要适量,因为高浓度的氧气往往会对人体造成伤害,引起氧中毒。
(1)氧气的化学性质比较活泼,具有较强的_____性。它能与人体内的葡萄糖反应生成二氧化碳和水,同时释放出能量供生命活动所需。写出该反应的文字表达式_____。
(2)我们有很多方法可以制取氧气,例如加热氯酸钾和二氧化锰的混合物,该反应的文字表达式为:_____,二氧化锰在其中的作用是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列反应属于置换反应的是( )
A. NH3+CO2+H2O=NH4HCO3
B. H2+CuO![]() Cu+H2O
Cu+H2O
C. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
D. HCl+AgNO3=AgCl↓+HNO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2020年1月25日总建筑面积为3.39万平方米的火神山医院正式开工,火神山医院在建造过程中用到/HDPE膜。HDPE膜具有极好的抗冲击性和防潮性,听完老师的描述后,同学们对HDPE膜的组成元素产生了浓厚的兴趣,进行了如下探究。
(提出问题)HDPE膜由什么元素组成?
(查阅资料)
①HDPE膜能够燃烧,燃烧可能生成一氧化碳。
②碱石灰主要成分是氢氧化钠固体和氧化钙固体。
(实验探究)如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在一定质量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D (装置中每步反应均进行完全)。
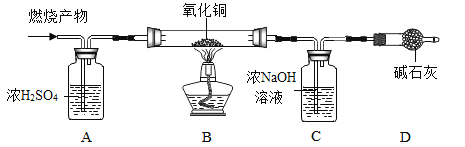
(实验记录)
装置质量 | A装置总质量 | C装置总质量 |
实验前 | 100.0g | 100.0g |
实验后 | 105.4g | 113.2g |
(实验分析)
(1)装置.A中浓硫酸的作用是___________。
(2)当观察到装置B中黑色粉末变成___色,可证明HDPE膜的燃烧产物中有_______。
(3)装置C中发生的化学反应方程式为________________。
(4)装置D的作用是________________。
(实验结论)
HDPE膜由元素_________(填元素符号)组成,它们的原子个数比为______。
(装置优化)
有同学认为,如若操作不当,C中溶液有可能会倒吸回B装置中,使得硬质玻璃管因骤冷而破裂为了降低实验风险,需要进行装置优化,请在方框中画出图像_________。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像不能正确反映对应变化关系的是
A.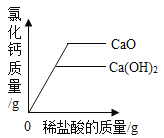 向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量
向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量
B.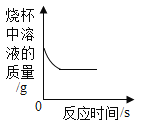 将锌片插入盛有一定质量稀硫酸的烧杯中
将锌片插入盛有一定质量稀硫酸的烧杯中
C.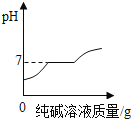 向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
D.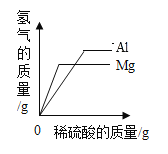 向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量
向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明同学将13.9g含杂质氯化钠的纯碱样品与140.5g稀盐酸相混合,充分反应,测得反应生成气体的质量(m)与反应时间(t)变化的曲线如下图所示:
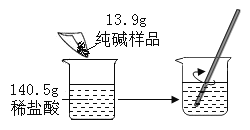
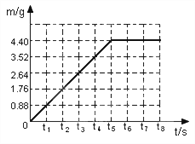
请计算:
(1)纯碱样品中碳酸钠的质量分数(计算结果保留一位小数);
(2)完全反应后所得溶液中溶质的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com